 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
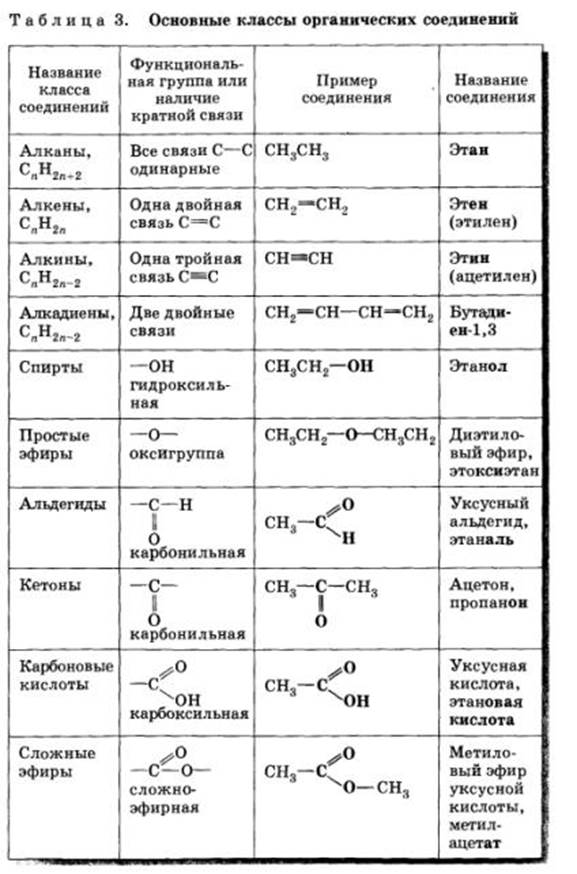
Классификация органических веществ по строению углеродной цепи и природе функциональных групп
|
|

3. Строение важнейших классов органических соединений: углеводородов, спиртов, тиоспиртов, фенолов, альдегидов, кетонов, карбоновых кислот, простых и сложных эфиров, аминов, амидов, нитросоединений.
| Гомологический ряд | Общая формула |
| Алканы | CnH2n+2 |
| Алкены | CnH2n |
| Алкины | CnH2n-2 |
| Диены | CnH2n-2 |
| Циклоалканы | CnH2n |
| Арены | CnH2n-6 |
| Моногалогеналканы | CnH2n+1X |
| Дигалогеналканы | CnH2n+X2 |
| Предельные одноатомные спирты | CnH2n+1OH или CnH2n+2O |
| Альдегиды | CnH2n+1COH или CnH2nO |
| Предельные одноосновные карбоновые кислоты | CnH2n+1СООH или CnH2nО2 |
| Простые эфиры | CnH2n+2О |
| Первичные амины | CnH2n+1NH2 или CnH2n+3N |
| Аминокислоты | (NH2)CnH2nCOOH |
| Трехатомный спирт | CnH2n-1(OH)3 |
| Сложные эфиры | CnH2nO2 |
| Тиоспирты | CnH2n+1SH |
| Тиоэфиры | CnH2n+2S |
| Нитросоединения | CnH2n+1NO2 |
| Амиды | СnH2n+1NR1R2 |
4. Номенклатура органических соединений: тривиальная, рациональная, международная. Принципы образования названий органических соединений по номенклатуре ИЮПАК.
В настоящее время для наименования органических соединений применяются три типа номенклатуры: тривиальная, рациональная и систематическая номенклатура — номенклатура IUPAC (ИЮПАК) — International Union of Pure and Applied Chemistry (Международного союза теоретической и прикладной химии).
Тривиальная (историческая) номенклатура — первая номенклатура, возникшая в начале развития органической химии, когда не существовало классификации и теории строения органических соединений. Органическим соединениям давали случайные названия по источнику получения (щавелевая кислота, яблочная кислота, ванилин), цвету или запаху (ароматические соединения), реже — по химическим свойствам (парафины). Многие такие названия часто применяются до сих пор. Например: мочевина, толуол, ксилол, индиго, уксусная кислота, масляная кислота, валериановая кислота, гликоль, аланин и многие другие.
Рациональная номенклатура — по этой номенклатуре за основу наименования органического соединения обычно принимают название наиболее простого (чаще всего первого) члена данного гомологического ряда. Все остальные соединения рассматриваются как производные этого соединения, образованные замещением в нем атомов водорода углеводородными или иными радикалами (например: триметилуксусный альдегид, метиламин, хлоруксусная кислота, метиловый спирт). В настоящее время такая номенклатура применяется только в тех случаях, когда она дает особенно наглядное представление о соединении.
Систематическая номенклатура — номенклатура IUPAC — международная единая химическая номенклатура. Систематическая номенклатура основывается на современной теории строения и классификации органических соединений и пытается решить главную проблему номенклатуры: название каждого органического соединения должно содержать правильные названия функций (заместителей) и основного скелета углеводорода и должно быть таким, чтобы по названию можно было написать единственно правильную структурную формулу.
Процесс создания международной номенклатуры был начат в 1892 г. (Женевская номенклатура), продолжен в 1930 г. (Льежская номенклатура), с 1947 г. дальнейшее развитие связано с деятельностью комиссии ИЮПАК по номенклатуре органических соединений.
При составлении названия вещества по его структурной формуле (и наоборот) необходимо последовательно выполнить следующие действия:
1. Найти основную (по старшинству) характеристическую группу и выбрать для нее обозначение в суффиксе.
2. Найти главную углеродную цепь (цикл), включающую основную характеристическую группу, и пронумеровать ее с того конца цепи, ближе к которому расположена старшая группа. Если таких возможностей несколько, то нужно учитывать наличие:
а) других характеристических групп (по старшинству);
б) двойной связи;
в) тройной связи;
г) других заместителей (по алфавиту).
3. К названию главной цепи добавить суффикс, обозначающий степень насыщенности связей. Если в молекуле несколько кратных связей, в суффиксе нужно указать их число, а после суффикса - арабскими цифрами их положение в углеродной цепи. Далее в суффикс включается название старшей характеристической группы с указанием ее положения арабской цифрой.
4. С помощью приставок (префиксов) обозначить заместители (боковые цепи, младшие характеристические группы) и расположить их по алфавиту. Положение заместителя нужно указать цифрой перед приставкой.
5. Расставить цифровые приставки, указывающие количество повторяющихся структурных элементов (они не учитываются при алфавитном размещении префиксов).
6. Расставить знаки препинания: все цифры отделить от слов дефисом, а друг от друга - запятыми.
5. Природа химических связей в органических соединениях: электронное строение соединений углерода, гибридизация орбиталей.
Представления о природе химической связи в органических соединениях впервые сформулировал Г.Льюис, предположивший, что атомы в молекуле связаны с помощью электронов: пара обобщенных электронов создает простую связь, а две или три пары образуют, соответственно, двойную и тройную связь. Рассматривая распределение электронной плотности в молекулах (например, ее смещение под влиянием электроотрицательных атомов O, Cl и др.) химики смогли объяснить реакционную способность многих соединений, т.е. возможность их участия в тех или иных реакциях.
Электронная формула: 1s22s22p2
1. Нормальное состояние атома углерода
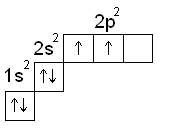
В нормальном состоянии атом углерода имеет степень окисления +2.
В данной степени окисления углерод образует оксид – СО
2. Возбужденное состояние атома углерода
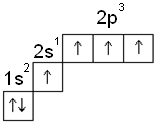
В возбужденном состоянии атом углерода имеет степень окисления +4.
В данной степени окисления углерод образует оксид – СО2
Электронное строение атома углерода определяет ряд особых свойств органических соединений. В частности, органические молекулы не образуют прочных кристаллических решеток, отличаются значительной подвижностью, и органические вещества способны растворяться друг в друге. Такоеэлектронное строение атома углерода обусловливает две характерных его особенности: возможность образовывать четыре ковалентные связи и неспособность к донорно-акцепторному взаимодействию.
Гибридизация орбиталей — гипотетический процесс смешения разных (s, p, d) орбиталей центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим характеристикам.
| Тип гибридизации | Число гибридных орбиталей | Геометрия | Структура | Примеры |
| sp | Линейная | 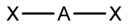
| BeF2, CO2, NO2+ | |
| sp2 | Треугольная | 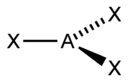
| BF3, NO3-, CO32- | |
| sp3 | Тетраэдрическая | 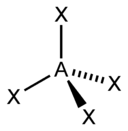
| CH4, ClO4-, SO42-, NH4+ | |
| dsp2 | Плоскоквадратная | 
| Ni(CO)4, [PdCl4]2- | |
| sp3d | Гексаэдрическая | 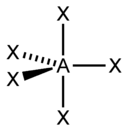
| PCl5, AsF5 | |
| sp3d2 | Октаэдрическая | 
| SF6, Fe(CN)63-, CoF63 |
!!!!!!!!!!!!!!!!!!Выберешь какие надо… Я думаю первых 3х будет достаточно))
6. Пространственное строение органических соединений. Конфигурация и конформация. Стереоизомеры: геометрические, оптические
Под изомерией понимают существование молекул с одинаковыми суммарными формулами, но различным строением или расположением атомов в пространстве. Химические и физические свойства изомерных веществ различны. Различают структурную и пространственную изомерию (стереоизомерия).
Структурная изомерия обусловлена различным расположением атомов в молекуле.
Возможны следующие виды структурной изомерии:
1) Изомерия углеродного скелета или изомерия цепи обусловлена различным порядком связи атомов, образующих скелет молекулы органических соединений.
2) Изомерия положения обусловлена различным расположением функциональных групп или кратных связей.
3)Изомерия функциональных групп (межклассовая изомерия)
4) Таутомерия – изомеры отличаются функциональными группами легко переходящими друг в друга.
А) Кето-енольная таутомерия
Б) Лактам- лактимная таутомерия
Дата публикования: 2015-11-01; Прочитано: 8550 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
