 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задачі першого рівня складності. 4B1 Знайти густину Гідрогену (Н2) при температурі 15°C і тиску 98 кПа
|
|
4B1 Знайти густину Гідрогену (Н2) при температурі 15°C і тиску 98 кПа. Молярна маса Гідрогену 2·10-3кг/моль.
R=8,31 Дж/(моль·К).
В) 0,082 кг/м3;
4B2 Газ, стиснутий ізотермічно від об'єму 8 л до 6 л. Тиск при цьому збільшився на 4 кПа. Який був початковий тиск?
А) 12 кПа;
4B3 При нагріванні ідеального газу, що знаходиться в закритій посудині на 2 К, його тиск збільшився у 2 рази. Обчислити початкову температуру газу.
Г) 2К;
4B4 Густина деякого газу 0,082 кг/м3 при тиску 100 кПа і температурі 17 ºС. Знайти середню квадратичну швидкість молекул газу.
А) 1900 м/с
4B5 В результаті нагрівання повітря на 3 К його об'єм збільшився на 1% від початкового значення. Знайти початкову температуру повітря. Тиск сталий.
В) 300 К;
4B6 Яка середня квадратична швидкість руху молекул деякого газу, якщо маючи масу 6 кг він займає об'єм 5м3 під тиском 200 кПа?
Б) 707 м/с;
4B7 В посудині об'ємом 4л знаходиться 1 г Гідрогену (Н2). Чому рівна його концентрація? 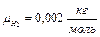 .
.
А) 7,5·1025 м-3;
4B8 Яка кількість молекул знаходиться в кімнаті об'ємом 80 м3 при температурі 17 ºС і тиску 100 кПа?
k=1,38·10-23 Дж/К.
В) 2·1027;
4B9 Знайти імпульс молекули азоту, яка летить із швидкістю 430 м/с.
Б) 2×10-23 кг∙м/с;
4B10 Знайти масу кисню, який знаходиться в балоні об’ємом 10 л і за температури –13 °С чинить тиск 9 МПа.
А) 1,32 кг;
4B11 Знайти відношення середніх квадратичних швидкостей молекул гелію та азоту, якщо ці гази мають однакову температуру.
Г) 6,25;
4B12 Яка кількість молекул міститься в кімнаті об’ємом 80 м3, якщо тиск повітря 100 кПа, а температура 17 °С?
Г) 2×1027;
4B13 Обсерваторія розташована на висоті 3250 м над рівнем моря. Знайти значення тиску на цій висоті, якщо температура повітря 5°С (вважати її постійною на всій висоті), молярна маса повітря 29×10-3 кг/моль, тиск на рівні моря вважати рівним 101,3 кПа.
Г) 67,2 кПа
4B14 Знайти середнє число зіткнень за одиницю часу молекул вуглекислого газу (СО2) при температурі 100 ºС, якщо середня довжина вільного пробігу дорівнює 870 нм, молярна маса вуглекислого газу дорівнює 44·10-3 кг/моль.
А) 4,9·108 с-1;
4B15 Знайти середню довжину вільного пробігу молекул повітря при нормальних умовах (р=105 Па, Т=273 К). Ефективний діаметр молекул повітря дорівнює 0,3 нм. Стала Больцмана k=1,38·10-23 Дж/К.
В) 94 нм;
4B16 Коефіцієнт дифузії і динамічної в’язкості Гідрогену (Н2) при деяких умовах рівні відповідно 1,42·10-4 м2/с і
8,5 мкПа·с. Знайти концентрацію Гідрогену. Молярна маса Гідрогену дорівнює 2·10-3 кг/моль. Число Авогадро N A=6,02·1023 1/моль.
В) 1,8·1025 м-3;
4B17 Вкажіть фізично правильне формулювання
Б) земну атмосферу покидають найбільше молекули легких газів, яких найбільше у верхніх шарах атмосфери і які мають найбільші швидкості;
4B18 Середня довжина вільного пробігу молекул даного газу
В) обернено пропорційно залежить від концентрації та ефективного діаметру цих молекул;
4B19 Вакуумом називають
В) такий стан розрідженого газу, коли молекули без зіткнень між собою можуть долати відстань від «стінки до стінки» посудини;
Дата публикования: 2015-11-01; Прочитано: 966 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
