 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Контактный метод получения серной кислоты
|
|
Рассмотрим процесс получения серной кислоты контактным методом из серного (железного) колчедана. Первой стадией процесса является окисление серного колчедана с получением обжигового газа, содержащего диоксид серы.
Обжиг колчедана (пирита) является сложным физико-химическим процессом и включает в себя ряд последовательно или одновременно протекающих реакций:
Термическая диссоциация 2FeS2 = 2FeS + S2;
Парофазное горение серы S2 + 2О2 = 2SО2;
Горение пирротина 4FeS + 7О2 = 2Fе2О3 + 4SО2.
Суммарная реакция: 4FеS2 + 11O2 = 2Fе2О3 + 8SО2. (I)
При небольшом избытке или недостатке кислорода образуется смешанный оксид железа:
3FеS2 + 8О2 = Fе3О4 + 6SО2.
Термическое разложение пирита начинается уже при температуре около 200 оС и одновременно воспламеняется сера. При температурах выше 680 °С интенсивно протекают все три реакции. В промышленности обжиг ведут при 850 - 900 °С. Лимитирующей стадией процесса становится массоперенос продуктов разложения в газовую фазу и окислителя к месту реакции. При тех же температурах твердый компонент размягчается, что способствует слипанию его частиц.
Реакция окисления SO2 экзотермична; тепловой эффект ее, как и любой химической реакции, зависит от температуры. В интервале 400—700 °С тепловой эффект реакции окисления (в кДж/моль) с достаточной для технических расчетов точностью может быть вычислен по формуле
Q= 10 142 —9.26Т или 24 205 — 2,21Т (в ккал/моль)
где Т — температура, К.
Реакция окисления SO2 в SO3 обратима. Константа равновесия этой реакции (в Па-0.5) описывается уравнением
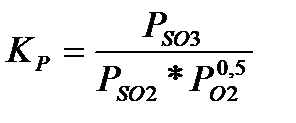
где Pso3, Pso2, Po2—равновесные парциальные давления SO3, SO2 и O2, Па.
Величина Кр зависит от температуры. Значения Kр в интервале
390—650°С могут быть вычислены по формуле
lgKp = 4905/T – 7,1479
Степень превращения SO2, достигаемая на катализаторе, зависит от его активности, состава газа, продолжительности контакта газа с катализатором, давления и др. Для газа данного состава теоретически возможная, т. е. равновесная степень превращения, зависит от температуры и выражается уравнением
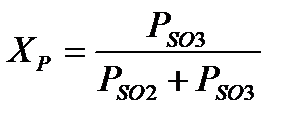
В производственных условиях существенное значение имеет скорость окисления SO2. От скорости этой реакции зависит количество диоксида серы, окисляющегося в единицу времени на единице массы катализатора, и, следовательно, расход катализатора, размеры контактного аппарата и другие технико-экономические показатели процесса. Процесс стремятся вести так, чтобы скорость окисления SO2, а также степень превращения были возможно более высокие.
Скорость окисления SO2 характеризуется константой скорости

где k0 —коэффициент; Е — энергия активации, Дж/моль; R —универсальная газовая постоянная, 8,31 Дж/(моль-К); Т — абсолютная температура, К.
Из кинетической теории газов известно, что доля молекул, обладающих энергией, достаточной для того, чтобы при их столкновении произошла реакция, составляет в первом приближении e~E/RT. Таким образом, этот член в уравнении скорости реакции характеризует долю эффективных столкновений, приводящих к образованию молекул SO3. Показатель степени в выражении e~ElRT отрицателен; следовательно, с повышением температуры скорость реакции возрастает, а с увеличением Е уменьшается.
Энергия активации Е реакции окисления SO2 в SO3 очень велика, поэтому без катализатора реакция гомогенного окисления практически не идет даже при высокой температуре. В присутствии твердых катализаторов энергия активации понижается, следовательно, скорость гетерогенной каталитической реакции возрастает. Таким образом, роль катализатора состоит в понижении энергии активации Е.
Важнейшей задачей в производстве серной кислоты является повышение степени превращения SО2 в SО3. Помимо увеличения производительности по серной кислоте выполнение этой задачи позволяет решить и экологические проблемы — снизить выбросы в окружающую среду вредного компонента SО2,.
Повышение степени превращения SО2 может быть достигнуто разными путями. Наиболее распространенный из них — создание схем двойного контактирования и двойной абсорбции (ДКДА).
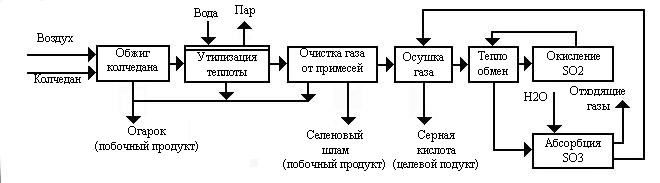
Рис.1. Функциональная схема производства серной кислоты из колчедана методом одинарного контактирования.
Дата публикования: 2015-10-09; Прочитано: 612 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
