 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Общие сведения. Серная кислота - H2SO4 (мол
|
|
Серная кислота - H2SO4 (мол. Масса 92,082) бесцветная маслянистая жидкость без запаха. Не дымит, в концентрированном виде не разрушает черные металлы, в то же время является одной из самых сильных кислот, в широком диапазоне температур (от -40…-20 до 260 – 336,5 ˚С) находится в жидком состоянии.
Области применения серной кислоты чрезвычайно обширны. Существенная ее часть используется как полупродукт в различных отраслях химической промышленности, прежде всего для получения минеральных удобрений, а также солей, кислот, взрывчатых веществ. Серная кислота применяется и при производстве красителей, химических волокон, в металлургической, текстильной, пищевой промышленности и т.д.
Серная кислота может существовать как самостоятельное химическое соединение H2SO4, а также в виде соединений с водой: H2SO4 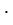 2H2O, H2SO4
2H2O, H2SO4 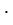 H2O, H2SO4
H2O, H2SO4 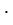 4H2O, H2SO4
4H2O, H2SO4 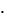 SO3, H2SO4
SO3, H2SO4 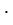 2SO3.
2SO3.
В технике серной кислотой называют безводную H2SO4 , ее водные растворы (смесь H2SO4 , H2O и H2SO4 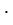 nH2O) и растворы триоксида серы в безводной H2SO4 – олеум (смесь H2SO4 и соединений H2SO4
nH2O) и растворы триоксида серы в безводной H2SO4 – олеум (смесь H2SO4 и соединений H2SO4 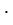 nSO3 ).
nSO3 ).
Безводная серная кислоты – тяжелая маслянистая бесцветная жидкость, смешивающаяся с водой и триоксидом серы в любом соотношении. Безводная 100%-ая серная кислота имеет сравнительно высокую температуру кристаллизации (10,7˚С).
Выпускают три вида серной кислоты:
| Концентрация | Температура кристаллизации, ˚С | |
| Башенная кислота | 75% | -29,5 |
| Контактная кислота | 92,5% | -22,0 |
| Олеум | 20% свободного SO3 | +2 |
Серная кислота и вода образуют азеотропную смесь: 98,3% H2SO4 и 1,7% H2O с максимальной температурой кипения (336,5 ˚С).
Дата публикования: 2015-10-09; Прочитано: 311 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
