 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
A) Уравнение скорости необратимых экзо- и эндотермических реакций
|
|
Вариант 8
1. Дайте определения возобновимых и невозобновимых, первичных и вторичных энергетических ресурсов
2. Для параллельных реакций
2А ¾® В (1)
А ¾® 2D (2)
имеем: nA,0 = 10 моль; nB,0 = nD,0 = 1 моль; nB = 3 моль; nD = 5 моль.
Рассчитать  ,
, 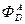 ,
, 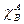 и
и 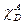 . Правильность решения проверить по
. Правильность решения проверить по 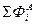 и
и  .
.
3. В реакторе идеального вытеснения проводят реакцию
k
А+2В à R+2S,
кинетика которой описывается уравнением WrA = kcA0.25 CB '7.75.
Определите объем реактора для достижения степени превращения реагента хA = 0,6, если k = 1,0 ч --1, CB.O= 0,8 кмоль/м3, с A.O= 0,6 кмоль/м3, объемный расход υ = 0,01м3/ч.
4. Элементарная (наименьшая) составная часть системы, сохраняющая все функциональные признаки БХТС и ХТС:
A) химическое производство B) физико-химическая система
C) химическая технология D) ХТП E) все ответы неверны
5. Pасходный коэффициент  :
:
A)  B)
B) 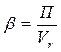 C)
C) 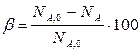
D) 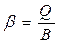 E)
E) 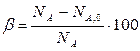
6. Процесс удаления влаги или другой жидкости из твердых материалов путем ее испарения и отвода образующегося пара
A) классификация B) измельчение C) сушка
D) обогащение E) выход концентрата
7. Явления в каком элементе ХТС не отображает технологический оператор химического превращения?
A) в реакторе B) в кристаллизаторе C) в конверторе
D) в струйном смесителе E) в автоклаве
8 Сколько существует классов метода параметрической идентификации:
A) 3 B) 4 C) 2 D) 8 E) 7
9. Какое из следующих уравнений верно?
А) χiA = FA,O * XA
B) χiA = ФiA * XA
C) χiA = FA * XA
D) χiA = FA,O * XA,O
E) χiA = ni,O * XA
10. Химические реакторы классифицируют по:
A) способу организации процесса B) режиму движения реакционной смеси
C) фазовому составу реакционной смеси D) температурному режиму
E) конструктивным особенностям реактора
11. Как увеличить поверхность соприкосновения фаз в системе двух несмешивающихся жидкостей.
A) Создать взвешенный слой подвижной эмульсии;
B) Увеличить перемешивание;
C) Повысить температуру;
D) Понизить температуру;
E) Повысить давления.
12. Какое уравнение приведено ниже?
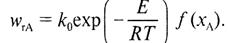
A) Уравнение скорости необратимых экзо- и эндотермических реакций
B) Уравнение скорости обратимых эндотермических реакций
C) Уравнение скорости необратимых экзотермических реакций
D) Уравнение скорости обратимых экзо- и эндотермических реакций
E) Уравнение материального баланса
13. Скорость гетерогенного процесса равна:
А) произведения константы скорости гетерогенного процесса К на концентрацию реагента А в газовой фазе Саg;
B) отношению константы скорости гетерогенного процесса К на концентрацию реагента А в газовой фазе Саg;
C) сумме константы скорости гетерогенного процесса К и концентрации реагента А в газовой фазе Саg;
D) разности константы скорости гетерогенного процесса К и концентраци реагента А в газовой фазе Саg;
E) нет правильного ответа.
Утвержден на заседании кафедры от 8 октября 2007 г. (протокол № 3)
Дата публикования: 2015-10-09; Прочитано: 243 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
