 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Гальванические преобразователи. Принцип работы pH-метра
|
|
Для характеристики растворов достаточно знать активность водородных ионов, которую для удобства записи и вычислений численно характеризуют отрицательным логарифмом активности ионов водорода - водородным показателем рН:
рН = -lg ан+ = -lg/н+ * сн+.
Приборы для измерения этого показателя получили название рН-метры. Они реализуют наиболее точный и универсальный метод измерения рН — электрометрический метод, т.е. определение электродных потенциалов различных электродов, помещенных в исследуемый раствор, содержащий водородные ионы.
Естественной входной величиной таких преобразователей является значение концентрации водородных ионов, выраженной в единицах рН, а выходной величиной — гальваническое напряжение, равное разности электродных потенциалов. Так как практически измерить потенциал одного электрода невозможно, то гальванический преобразователь всегда состоит из двух полуэлементов — измерительного электрода, помещенного в исследуемый раствор, и образцового (вспомогательного) полуэлемента (рис. 2.49).
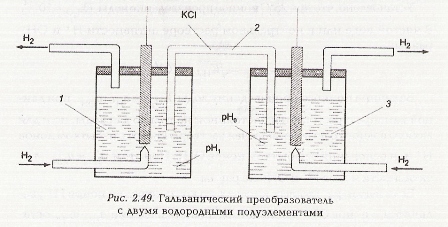
На рис. 2.49 один из двух водородных электродов (измерительный) помещается в исследуемый раствор 1, который при помощи электролитического ключа 2 соединяется с нормальным электродным полуэлементом 3, содержащим электролит с активностью водородных ионов ан+)2=1 г*экв/л.
Дата публикования: 2015-10-09; Прочитано: 525 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
