 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Взаимодействие кислот с металлами
|
|
При взаимодействии соляной и разбавленной серной кислот с металлами окислителем является катион водорода Н+, поэтому они взаимодействуют с металлами, стоящими в ряду напряжений до водорода.
Mg + 2HCl = MgCl2 + H2#; Mg + H2SO4(разб.) = MgSO4 + H2#
Металлы переменной валентности соляной и разбавленной серной кислотами окисляются до низших степеней окисления. Железо имеет наиболее распространенные степени окисления +2 и +3. При реакции с этими кислотами железо окисляется до степени окисления +2.
Fe + 2HCl = FeCl2 + H2#
Свинец является более активным элементом, чем водород, но в процессе реакции на его поверхности образуется плотная нерастворимая пленка хлорида или сульфата свинца(II) и реакция практически не протекает.
В концентрированной серной кислоте окислителем является сульфат ион 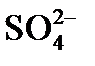 , в котором сера находится в степени окисления +6. При реакции с металлами серная кислота восстанавливается до сероводорода (H2S), серы (S) и оксида серы(IV) (SO2). Продукты восстановления серной кислоты зависит от активности металла.
, в котором сера находится в степени окисления +6. При реакции с металлами серная кислота восстанавливается до сероводорода (H2S), серы (S) и оксида серы(IV) (SO2). Продукты восстановления серной кислоты зависит от активности металла.
При взаимодействии концентрированной серной кислоты с активными металлами  образуется соль, вода и преимущественно сероводород. φ0(К/К+) = -2,92В – активный металл.
образуется соль, вода и преимущественно сероводород. φ0(К/К+) = -2,92В – активный металл.
8К + 5H2SO4(конц.) = 4К2SO4 + H2S# +4H2O.
Малоактивные металлы восстанавливают серную кислоту преимущественно до SO2. φ0(Ag/Ag+) = +0,8В – неактивный металл.
2Ag + 2H2SO4(конц.) = Ag2SO4 + SO2# +2H2O
Металлы средней активности  восстанавливают серную кислоту преимущественно до S. φ0(Сd/Cd2+) = – 0,40В –металл средней активности.
восстанавливают серную кислоту преимущественно до S. φ0(Сd/Cd2+) = – 0,40В –металл средней активности.
3Cd + 4H2SO4(конц.) = 3CdSO4 + S$ +4H2O
Металлы переменной валентности окисляются концентрированной серной кислотой, как правило, до высшей степени окисления.
3Sn + 8H2SO4(конц.) = 3Sn(SO4)2 + 2S$ +8H2O
Благородные металлы (Au, Pt и некоторые другие) с концентрированной серной кислотой не взаимодействуют ни при каких условиях. Некоторые металлы (Al, Fe, Cr, Ni и др.) не взаимодействуют с концентрированной серной кислотой при обычных условиях (пассивируются), но взаимодействуют при нагревании. Это свойство железа позволяет хранить и перевозить концентрированную серную кислоту в емкостях из обычной стали.
Свинец с концентрированной серной кислотой взаимодействует с образованием растворимой кислой соли.
Pb + 3H2SO4(конц.) = Pb(HSO4)2 + SO2# +2H2O
В азотной кислоте, независимо от ее концентрации, окислителем является нитрат-ион  , содержащий азот в степени окисления +5, поэтому водород не выделяется, а только продукты восстановления азотной кислоты: NH4NO3, N2, N2O, NO, HNO2, NO2. Свободный аммиак не выделяется, т.к. он взаимодействует с азотной кислотой, образуя нитрат аммония NH4NO3.
, содержащий азот в степени окисления +5, поэтому водород не выделяется, а только продукты восстановления азотной кислоты: NH4NO3, N2, N2O, NO, HNO2, NO2. Свободный аммиак не выделяется, т.к. он взаимодействует с азотной кислотой, образуя нитрат аммония NH4NO3.
При взаимодействии металлов с концентрированной азотной кислотой продуктом ее восстановления является преимущественно NO2, независимо от природы металла.
Mg + 4HNO3(конц.) = Mg(NO3)2 + NO2# +2H2O
При реакции выделяется бурый газ NO2

Zn + 4HNO3(конц.) = Zn(NO3)2 + NO2# +2H2O

Cu + 4HNO3(конц.) = Cu(NO3)2 + NO2# +2H2O
При опускании кусочка меди в концентрированную азотную кислоту выделяется бурый газ, а на дне образуется голубой раствор нитрата меди(II)



Металлы переменной валентности при взаимодействии с концентрированной азотной кислотой окисляются до высшей степени окисления, а металлы, которые окисляются до степени окисления +4 и выше, образуют кислоты или оксиды.
Sn + 4HNO3(конц.) = H2SnO3 + 4NO2# +H2O
2Sb + 10HNO3(конц.) = Sb2O5 + 10NO2# +5H2O
Mo + 6HNO3(конц.) = H2MoO4 + 6NO2# +2H2O
В концентрированной азотной кислоте пассивируются Al, Fe, Cr, Ni, Со и некоторые другие металлы. После обработки азотной кислотой эти металлы не реагируют и с другими кислотами.
При взаимодействии металлов с разбавленной азотной кислотой продукт ее восстановления зависит от активности металла: чем активнее металл, тем в большей степени восстанавливается азотная кислота.
Активные металлы восстанавливают азотную кислоту максимально.
8Na + 10HNO3(разб.) = 8КNO3 + NH4NO3 +3H2O
Продуктами восстановления разбавленной азотной кислоты металлами средней активности являются азот или оксид азота(I).
4Cd + 10HNO3(разб.) = 4Cd(NO3)2 + N2O# +5H2O
5Mn + 12HNO3(разб.) = 5Mn(NO3)2 + N2# +6H2O
При взаимодействии разбавленной азотной кислоты с малоактивными металлами продуктом восстановления является оксид азота(II).
3Cu + 8HNO3(разб.) = 3Cu(NO3)2 + 2NO# +4H2O
Надо обратить внимание, что при реакции с азотной кислотой получается смесь соединений азота, но мы записываем то соединение, которое получается в большем количестве.
Основное правило: чем выше активность металла и ниже концентрация азотной кислоты, тем ниже степень окисления азота в том соединении, которое образуется больше других.
Для окисления золота, платины и других благородных металлов используется смесь концентрированных азотной и соляной кислот, называемая «царской водкой». В этой смеси образуется очень сильный окислитель - атомарный хлор:
HNO3 + 3HCl = NOCl + Cl2 + 2H2O
NOCl = NO + Cl
и повышается восстановительная активность металлов вследствие образования комплексов, поэтому окисление благородных металлов происходит с образованием комплексных кислот:
Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O
3Pt + 2HNO3 + 12HCl = 3H2[PtCl4] + 2NO + 4H2O
Некоторые металлы Nb, Ta, W не растворяются даже в «царской водке», но растворяются в смеси азотной и фтороводородной кислот.
3Ta + 5HNO3 + 21HF = 3H2TaF7 + 5NO + 10H2O
W + 2HNO3 + 8HF = H2WF8 + 2NO + 4H2O
2.7. Характерные химические свойства солей: средних, кислых, основных, комплексных (на примере соединений алюминия и цинка)
Солями называются соединения, состоящие из катионов металлов (или аммония) и кислотных остатков. Соли можно рассматривать как продукт взаимодействия кислоты и основания при этом могут получаться нормальные (средние), кислые и основные соли.
Нормальные соли образуются в том случае, когда количеств кислоты и основания достаточно для полного взаимодействия.
Н3РО4 + 3КОН = К3РО4 + 3Н2О
Кислые соли образуются при недостатке основания, когда катионов металла недостаточно для замещения всех катионов водорода в молекуле кислоты.
Н3РО4 + 2КОН = К2НРО4 + 2Н2О
Н3РО4 + КОН = КН2РО4 + Н2О
В кислых солях в составе кислотных остатков содержится водород. Кислые соли возможны для многоосновных кислот и невозможны для одноосновных.
Основные соли образуются при недостатке кислоты, когда анионов кислотных остатков недостаточно для полного замещения всех гидроксогрупп в основании.
Cr(OH)3 + HNO3 = Cr(OH)2NO3 + H2O
Cr(OH)3 + 2HNO3 = CrOH(NO3)2 + 2H2O
В основных солях в составе катионов содержатся гидроксогруппы. Основные соли возможны для многокислотных оснований (содержат две и больше ОН-группы) и невозможны для однокислотных.
Некоторые основные соли самопроизвольно разлагаются с выделением воды, при этом образуются оксосоли.
Sb(OH)2Cl = SbOCl + H2O
Bi(OH)2NO3 = BiONO3 + H2O
Оксосоли обладают всеми свойствами основных солей.
Многие соли в твердом состоянии являются кристаллогидратами: CuSO4.5H2O; Na2CO3.10H2O и т.д.
Дата публикования: 2015-10-09; Прочитано: 5054 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
