 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Национальный исследовательский Томский политехнический университет, г. Томск, Россия
|
|
ВЛИЯНИЕ КОНЦЕНТРАЦИИ И ПЛОТНОСТИ ТОКА НА СКОРОСТЬ ЭЛЕКТРОХИМИЧЕСКОГО ОКИСЛЕНИЯ КАДМИЯ
А.В.Скобелкина, С.Е. Пугачева, А.С. Долинина
Научный руководитель доцент Д.А.Горлушко
Национальный исследовательский Томский политехнический университет, г. Томск, Россия
В последние годы большое применение находят высокодисперсным материалам (нанопорошкам), обеспечивающим прогресс в материаловедении. Уникальные свойства наноматериалов зависят как от особенностей отдельных частиц (кристаллитов), так и их взаимодействия между ними. Основной характеристикой нанокристаллических материалов является дисперсность. Структура высокодисперсных материалов зависит от способа получения. Эффективным методом изменения структурных характеристик твердого тела является уменьшение размеров зерен. Разнообразие уникальных свойств нанопорошков связано со специфическим характером состояний атомов и электронов в малых частицах (1-10 нм), являющихся основными морфологическими элементами ультрадисперсных сред, и увеличением доли их поверхностного вклада в общие свойства системы [1]. Известно несколько способов получения высокодисперсных порошков оксидов металлов, такие как плазмохимический синтез, метод осаждения, золь-гель метод, метод восстановления и термического разложения, электрохимический метод.
Целью работы является исследование кинетики разрушения кадмия при его электрохимическом окислении под действием переменного тока в растворах хлорида натрия, определение оптимальных параметров проведения процесса для наибольшего выхода продукта. В результате реакции образуется оксид кадмия, который находит широкое применение во многих отраслях [2]:
- используют при нанесении антикоррозионных покрытий на металлы, применяемые в судостроении, авиации и автомобильной промышленности;
- в гальванотехнике;
- кадмиевые электроды используют в аккумуляторах;
- оксид кадмия является катализатором для реакций гидрогенизации и дегидрогенизации;
- используется как компонент при производстве специальных стекол, антифрикционных, легкоплавких и ювелирных сплавов.
Исследование кинетики электрохимического окисления кадмия с использованием переменного тока промышленной частоты проводилось согласно методике, изложенной в [3]. На скорость процесса образования оксида кадмия наибольшее влияние оказывают следующие факторы: плотность переменного тока, состав и концентрация электролита и температура электролиза. Одним из основных факторов, влияющих на процесс электрохимического окисления металла на переменном токе, является концентрация электролита. Вместе с тем большое влияние на скорость процесса оказывает плотность переменного тока. Были проведены опыты электрохимического окисления кадмия в растворе хлорида натрия при различных концентрациях(3%, 5%, 10%, 15%, 20% и 25%) и плотностях тока 1 А/см2, 2 А/см2 и 3А/см2. Температура проведения процесса поддерживалась постоянная и равна 95оС. При проведении исследований в качестве объектов были использованы кадмий марки Кд0 ГОСТ 1467 - 93[4] (материал электродов) и натрий хлористый ГОСТ 4233-77 [5](растворы электролита).
С целью определения зависимости скорости разрушения кадмия под действием переменного тока от концентрации раствора электролита проводились эксперименты, в которых использовались растворы, содержащие от 3 до 25% масс. хлорида натрия и при постоянной температуре. Верхний концентрационный предел обусловлен пределом растворимости хлорида натрия в воде.
Следует отметить, что при плотности тока 1 А/см2 электрохимическое окисление кадмия под действием переменного тока протекает с низкой скоростью, вследствие чего проведение процесса при плотности тока менее 1 А/см2 является нецелесообразным. При плотности тока равной 3 А/см2 наблюдается быстрый разогрев электролита, особенно при низких концентрациях раствора. Это требует в ряде случаев интенсивного охлаждения системы во избежание повышения ее температуры до температуры кипения раствора.
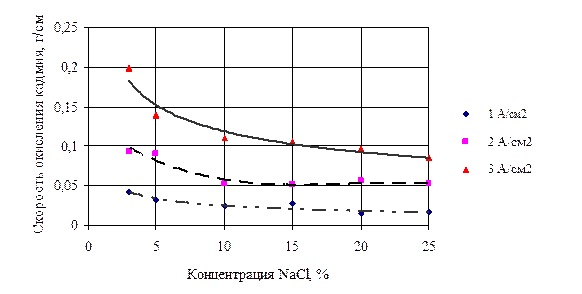
По результатам эксперимента были построены зависимости скорости окисления кадмия от концентрации, представленные на рисунке ниже.
Из рисунка следует, что с уменьшением концентрации раствора хлорида натрия, скорость разрушения кадмия возрастает. Максимальная скорость разрушения кадмия наблюдается при концентрации хлорида натрия 3%. При высоких концентрациях раствора хлорида натрия скорость окисления кадмия мала. При разных плотностях тока наибольшее значение скорости окисления достигается при минимальной концентрации – 3%. Увеличение плотности тока также приводит росту скорости окисления. Так максимальное значение скорости окисления кадмия достигается при концентрации хлорида натрия равной 3 % и плотности тока 3А/см2 и равно 0,2 г/см2ч. Минимальное значение скорости окисления наблюдается при наибольшей концентрации электролита – 25 % и наименьшей плотности тока – 1 А/см2 и равно 0,02 г/см2ч. Подобные зависимости скорости разрушения электродов от плотности тока и концентрации электролита наблюдаются при электрохимическом окислении кадмия и меди в растворах хлорида аммония и хлорида натрия [6, 7], меди в растворах хлорида калия [8], а также для олова в растворах хлоридов калия, натрия, аммония и ацетата натрия [9].
Дата публикования: 2015-10-09; Прочитано: 268 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
