 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Получение оснований
|
|
| щелочи | Нерастворимые основания |
| Щелочной оксид + вода K2O + H2Oà 2KOH BaO + H2OàBa(OH)2 Щелочной металл + вода 2Na +2 H2Oà 2NaOH + H2↑ Ca + 2H2Oà Ca(OH)2 + H2↑ | Соль + щёлочь = Нерастворимое основание + другая соль 2КOH+ FeSO4à Fe(OH)2 ↓ + К2SO4 |

| Тема «Понятие об амфотерности. Амфотерные оксиды и гидроксиды» |
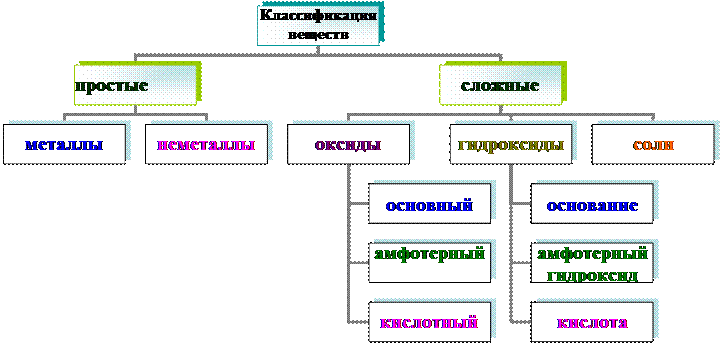
АМФОТЕРНОСТЬ – это способность (в зависимости от условий) проявлять или кислотные, или основные свойства. К амфотерным относятся некоторые металлы, их оксиды и гидроксиды.
Например, Al Al2O3 Al(OH)3 ; Zn ZnO Zn(OH)2 и др.
| При взаимодействии с кислотами проявляют основные свойства | Al2O3 + 6HCl à 2AlCl3 + 3H2O | ZnO + 2HCl à ZnCl2 + H2O |
| 2Al(OH)3 + 3H2SO4 àAl2(SO4)3 + +6H2O | Zn(OH)2 + H2SO4àZnSO4 +2H2O | |
| При взаимодействии с основаниями (со щелочами) проявляют кислотные свойства !!!При составлении формулы соли следует учитывать, что оксидам и основаниям соответствуют кислоты: HAlO2 – алюминиевая (соль алюминат) H2ZnO2 – цинковая (соль - цинкат) | Al2O3 + 2NaOH à 2NaAlO2 + +H2O | ZnO+ 2NaOH à Na2ZnO2 + +H2O |
| Al(OH)3 + KOH à KAlO2 + 2H2O | Zn(OH)2+2KOHà K2ZnO2 +2H2O |
Как составить формулу соли?
Соль – сложное вещество, состоящее из атомов металла (Ме), связанного с кислотным остатком (КО)
Вспомните составление формул по валентности:
| I I МеКО | II II МеКО | III III МеКО |
| I II Ме2КО | II I Ме(КО)2 | III I Ме(КО)3 |
| I III Ме3КО | II III Ме3(КО)2 | III II Ме2(КО)3 |
 Валентность металла надо запомнить
Валентность металла надо запомнить
 Валентность кислотного остатка определяется числом атомов водорода в формуле кислоты
Валентность кислотного остатка определяется числом атомов водорода в формуле кислоты
Дата публикования: 2015-10-09; Прочитано: 217 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
