 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Нақты газдың тәжірибелік изотермасын көрсетіңіз. 1 страница
|
|
Молекулалық физика
Тест
1. Газ молекулаларының қозғалыс сипаты:
A) Газдардағы молекулалар қозғалмайды.
B) Газдардағы молекулалар тек тербелмелі қозғалысқа қатысады.
C) Газдардағы молекулалар тек айналмалы қозғалысқа қатысады
D) Газдардағы қозғалмайтын молекулалар бір-біріне тығыз орналасқан.
E) Газдардағы молекулалар жылулық хаостық қозғалысқа қатысады. +
2. СИ жүйесіндегі 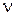 моль санының өлшемі:
моль санының өлшемі:
A) 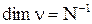
B) 
C) 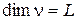
D) 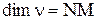
E) 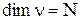 +
+
3. СИ жүйесіндегі көлемнің өлшемі:
A) 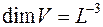
B) 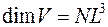
C) 
D)  +
+
E) 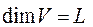
4. СИ жүйесіндегі тығыздықтың өлшемі:
A) 
B) 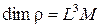
C) 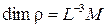 +
+
D) 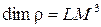
E) 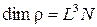
5. Термодинамикалық температураның Т Цельсий шкаласындағы t температурамен байланысы
A) T= t - 273,150
B) T= t + 273,15 +
C) T= t/ 273,15
D) T= 273,15 - t
E) t = T + 273,15.
6. Газдардағы молекулалардың орташа еркін жүру жолының ұзындығы мен эффективтік диаметрінің арасындағы қатынас:
A) Газдарда молекулалардың эффективтік диаметрі молекулалардың орташа еркін жүру жолының ұзындығынан өте кіші. +
B) Газдарда молекулалардың эффективтік диаметрі молекулалардың орташа еркін жүру жолының ұзындығынан үлкен.
C) Газдарда молекулалардың эффективтік диаметрі молекулалардың орташа еркін жүру жолының ұзындығынан екі есе үлкен.
D) Газдарда молекулалардың эффективтік диаметрі молекулалардың орташа еркін жүру жолының ұзындығынан өте үлкен.
E) Газдарда молекулалардың эффективтік диаметрі молекулалардың орташа еркін жүру жолының ұзындығына тең.
7. Больцман тұрақтысының универсал газ тұрақтысымен байланысы:
A)  +
+
B) 
C) 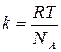
D) 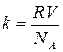
E) 
8. СИ жүйесіндегі Больцман тұрақтысының өлшем бірлігі:
A) К / Дж
B) Дж
C) Дж/К кг
D) Дж/К м
E) Дж/К +
9. СИ жүйесіндегі универсал газ тұрақтысының өлшем бірлігі:
A) К /(моль Дж)
B) Дж/(кг К)
C) Дж кг/ моль
D) Дж/(моль К) +
E) Дж моль К
10. Идеальный газ дегеніміз...
А) молекулалары бір-бірімен әрекеттеспейтін материальдық нүктелер ретінде қарастырылатын газ; +
В) молекулалары бір-бірімен әрекеттеспейтін қатты сфералар ретінде қарастырылатын газ;
С) молекулалары материальдық нүктелер ретінде қарастырылатын, ал өзара тебу күштері арақашықтыққа кері пропорционал газ;
D) молекулалары материальдық нүктелер ретінде қарастырылатын, ал өзара тартылыс күштері арақашықтыққа кері пропорционал газ;
E) молекулалары қатты сфералар ретінде қарастырылатын, ал өзара тартылыс күштері арақашықтыққа тура пропорционал газ;
11. Газдардың молекула - кинетикалық теориясының негізгі теңдеуінің дұрыс түрін көрсетіңіз (n – бірлік көлемдегі бөлшектер саны).
A) 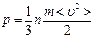 ;
;
B) 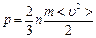 ; +
; +
C) 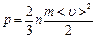 ;
;
D) 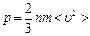 ;
;
E) 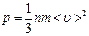 .
.
12. Газдардың молекула - кинетикалық теориясының негізгі теңдеуінің дұрыс формуласын көрсетіңіз (<Eк> - газдағы бір молекуланың жылулық қозғалысының орташа кинетикалық энергиясы).
A) 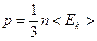 ;
;
B) 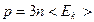 ;
;
C) 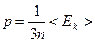 ;
;
D) 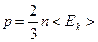 ; +
; +
E) 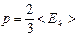 .
.
13. Идеал газдың қысымы қалай өзгереді, егер молекулаларының орташа квадраттық жылдамдығы 1,5 есе өссе, ал молекулалардың сандық тығыздығы өзгермесе?
A) 1,5 есе өседі;
B) 2,25 есе өседі; +
C) өзгермейді;
D) 1,5 есе кемиді;
E) 2,25 есе кемиді.
14. Идеал газдың қысымы қалай өзгереді, егер молекулаларының сандық тығыздығы үш есе артып, ал молекулалардың орташа квадраттық жылдамдығы өзгермесе?
A) үш есе кемиді;
B) өзгермейді;
C) екі есе артады;
D) үш есе артады; +
E) екі есе кемиді.
15. Идеал газ тығыздығының дұрыс өрнегі:
A) 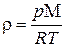 +
+
B) 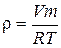
C) 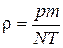
D) 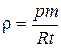
E) 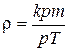
16. Молекула массасы 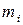 арқылы идеал газдың тығыздығы арқылы есептелінетін өрнек:
арқылы идеал газдың тығыздығы арқылы есептелінетін өрнек:
A) 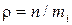
B) 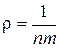
C) 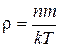
D) 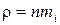 +
+
E) 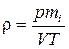
17. Идеал газдың күй теңдеуі қалыпты жағдайда ауа тығыздығының қандай мәнін береді:
A) 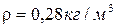
B) 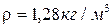 +
+
C) 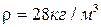
D) 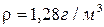
E) 
18. Идеал газ молекулаларының сандық тығыздығы қандай өрнек арқылы табылады:
A) 
B) 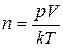
C) 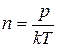 +
+
D) 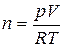
E) 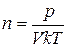
19. Температурасы Т=600 К, қысымы 200 Па бір куб метр көлемдегі азоттың қанша молекуласы бар:
A) 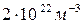 +
+
B) 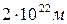
C) 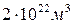
D) 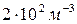
E) 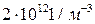
20. Егер идеал газдың тығыздыңы 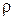 белгілі болса, онда белгілі температурадағы T және қысымдағы p, молярлық массаны
белгілі болса, онда белгілі температурадағы T және қысымдағы p, молярлық массаны 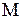 келесі формуламен табуға болады:
келесі формуламен табуға болады:
A) 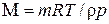
B) 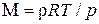 +
+
C) 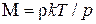
D) 
E) 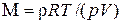
21. Егер идеал газдың тығыздыңы 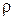 белгілі болса, онда белгілі температурадағы T және қысымдағы p, бір молекуланың массасын
белгілі болса, онда белгілі температурадағы T және қысымдағы p, бір молекуланың массасын 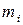 келесі формуламен табуға болады:
келесі формуламен табуға болады:
A)  +
+
B) 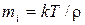
C) 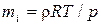
D) 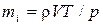
E) 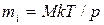
22. Екі идеал қоспасының тығыздығын осы газдар молекулаларының массалары 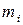 арқылы түрін анықтаңыз:
арқылы түрін анықтаңыз:
A) 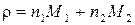
B) 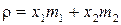
C) 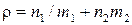
D)  +
+
E) 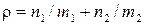
23. Термодинамикалық жүйенің ішкі энергиясы
A) Жылу процестеріндегі өзгеретін жүйенің толық энергиясының бір бөлігі. +
B) Жылу процестеріндегі туындайтын жүйенің толық энергиясының бір бөлігі.
C) Жылу процестеріндегі жойылатын жүйенің толық энергиясының бір бөлігі.
D) Жылу процестеріндегі кететін жүйенің толық энергиясының бір бөлігі.
E) Жылу процестеріндегі өзгермейтін жүйенің толық энергиясының бір бөлігі.
24. Термодинамикалық жүйенің ішкі энергиясын өзгертетін себебтер
A) Себебі энергияның тууындауы және жойылуы.
B) Себебі жүйе энергиясының жойылуы.
C) Себебі жүйеге сырттан жұмыс және жылу арқылы әсер ету. +
D) Себебі жүйедегі энергияның пайда болуы.
E) Себебі жүйедегі энергия көздері.
25. Үш компонентті идеал газ қоспасы үшін Дальтон заңының жазылуы:
A) 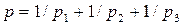
B)  +
+
C) 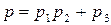
D) 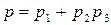
E) 
26. 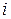 еркіндік дәрежесі бар газ молекуласының орташа энергиясы:
еркіндік дәрежесі бар газ молекуласының орташа энергиясы:
A) 
B) 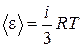
C) 
D) 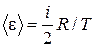
E) 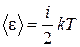 +
+
27. Қатты байланыстағы үш атомды молекулалардың еркіндік дәрежелерінің саны:
A) і =7/2
B) і =5
C) і =5
D) і =5
E) і =6 +
28. Термодинамикалық жүйенің ішкі энергиясы
A) Термодинамикалық жүйенің ішкі энергиясы күш өрісіндегі жүйенің кинетикалық және потенциальдық энергияларының қосындысы.
B) Термодинамикалық жүйенің ішкі энергиясы жүйедегі барлық микробөлшектердің жылулық қозғалысының кинетикалық энергиясы мен өзара әрекеттесуінің потенциальдық энергияларынан тұрады. +
C) Термодинамикалық жүйенің ішкі энергиясы тұтас жүйе айналуының кинетикалық энергияларынан тұрады.
D) Термодинамикалық жүйенің ішкі энергиясы сыртқы өрістегі жүйенің барлық потенциальдық энергияларының қосындысы.
E) Термодинамикалық жүйенің ішкі энергиясы сыртқы күштер жұмысынан тұрады.
29. Термодинамиканың бірінші бастамасы:
A)  +
+
B) 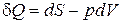
C) 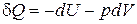
D) 
E) 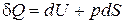
30. Термодинамиканың бірінші бастамасының дұрыс тұжырымдамасы:
A) Механикалық процестердегі энергияның сақталу және түрлену заңы.
B) Жүйенің ілгерілемелі қозғалысы кезіндегі энергияның сақталу және түрлену заңы.
C) Жылу процесіндегі энергияның сақталу және түрлену заңы. +
D) Процестердегі энергияның барлық түрлерінің сақталу және түрлену заңы.
E) Жылу процестеріндегі энергияның өсу заңы.
31. Неліктен жылу мөлшері 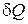 толық дифференциал емес?
толық дифференциал емес?
A) Жылу күй функциясы, себебі процестің функциясы емес.
B) Жылу күй функциясы емес және процестерде жойылады.
C) Жылу күй функциясы және процестерде жойылады.
D) Себебі жылу тек жылу процестерінде пайда болады.
E) Жылу күй функциясы емес, себебі процестің функциясы. +
32. Неліктен денелерде қанша жылу барын анықтау мүмкін емес
A) Себебі жылудың кетуі мүмкін.
B) Себебі жылу әртүрлі күйлерде бірдей емес.
C) Себебі жылу жойылмайды.
D) Себебі жылу күй функциясы.
E) Себебі жылу күй функциясы емес. +
33. Қайтымды процестегі күй функциясының өсімшесі.
A) Күй функциясының өсімшесі процестегі оны өндірудің айырымы ретінде анықталады.
B) Күй функциясының өсімшесі процестің басындағы және соңындағы мәндерінің қатынасы арқылы анықталады.
C) Күй функциясының өсімшесі процестің басындағы және соңындағы өндірілген мәндерінің көбейтіндісі арқылы анықталады.
D) Күй функциясының өсімшесі процестің басындағы және соңындағы мәндерінің қосындысы арқылы анықталады.
E) Күй функциясының өсімшесі процестің басындағы және соңындағы мәндерінің айырымы арқылы анықталады. +
34. Тұрақты көлемдегі (Не) гелийдің молярлық жылусиымдылығы тең:
A) 120 кДж/(моль К)
B) 2,5 Дж/моль К
C) 1,2 кДж/(моль К)
D) 12 Дж/(кмоль К)
E) 12 Дж/(моль К) +
35. Адиабаталық процесс
A) Жүйедегі жылу тұрақты болғандағы өтетін процесс.
B) Бұл процесте температура өзгермейді.
C) Бұл процесте сыртқы денелер жұмыс жасамайды.
D) Бұл процесте ішкі энергия өзгермейді.
E) Бұл процесте жүйе сыртқы ортамен жылуалмаспайды. +
36. Изотермдік процестегі алынған жылу жұмсалады?
A) Жылуды өзгертуге.
B) Жұмыс жасауға. +
C) Ішкі энергияны өзгертуге.
D) Жүйенің құрылымын өзгертуге.
E) Жылусиымдылықты өзгертуге.
37. Адиабатаның теңдеуі:
A) 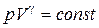 +
+
B) 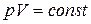
C) 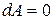
D) 
E) 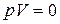
38. Изотермдік процестегі жүйенің істейтін жұмысы қайда жұмсалады?
A) Барлық жұмыс жылу түрінде термостатқа беріледі. +
B) Ішкі энергияны арттыруға және жұмыс жасауға.
C) Ішкі температураны арттыруға және жұмыс жасауға.
D) Барлық жұмыс жүйенің массасын арттыруға жұмсалады.
E) Барлық жұмыс жүйенің моль санын арттыруға жұмсалады.
39. Адиабаталық процестегі жұмыс қайда жұмсалады?
A) Барлық жұмыс жүйенің моль санын арттыруға жұмсалады.
B) Жұмыс жүйенің массасын арттыруға жұмсалады.
C) Барлық жұмыс жүйенің ішкі энергиясын арттыруға жұмсалады. +
D) Барлық жұмыс жүйенің жылусиымдылығын арттыруға жұмсалады.
E) Барлық жұмыс жүйенің жылуын арттыруға жұмсалады.
40. Карно циклы қандай процестерден құралады?
A) Қайтымды адиабата мен қайтымсыз изотермадан.
B) Екі қайтымды изобара мен екі қайтымсыз изотермадан.
C) Екі қайтымды изотерма мен екі қайтымсыз адиабатадан.
D) Екі қайтымды изотерма мен екі қайтымсыз адиабатадан. +
E) Екі қайтымды изохора мен екі қайтымды адиабатадан.
41. Карно циклындағы қолданылатын қыздырғыштың жылусиымдылығы қандай?
A) Жылусиымдылығы нөлге тең.
B) Жылусиымдылығы изобарлық жылусиымдылыққа тең.
C) Жылусиымдылығы изохоралық жылусиымдылыққа тең.
D) Жылусиымдылығы молярлық жылусиымдылыққа тең.
E) Жылусиымдылығы шексіздікке тең. +
42. Термодинамиканың екінші бастамасын қалай тұжырымдауға болады?
A) Жылутасымалдаудың өздігінен жүрмейтіндігі.
B) Температурасы жоғары денеден жылутасымалының температурасы төмен денеге өздігінен жүрмейтіндігі.
C) Температурасы жоғары денеден жылутасымалының температурасы төмен денеге өздігінен жүру мүмкіндігі.
D) Температурасы төмен денеден жылутасымалының температурасы жоғары денеге өздігінен жүрмейтіндігі. +
E) Температурасы төмен денеден жылутасымалының температурасы жоғары денеге өздігінен жүрмейтіндігі.
43. Кельвин принципі қалай тұжырымдалады?
A) Бірнеше қыздырғыштан алынған жылу арқылы жасалған жұмыс циклы мүмкін емес.
B) Бірнеше қыздырғыштан алынған жылу арқылы жасалған жұмыс жалғыз нәтижесі болатын циклы мүмкін емес.
C) Нәтижесі қыздырғыштан алынған жылудың мұздатқышқа беретін циклдық процесс мүмкін емес.
D) Сыртқы ортадан алынған жұмыс арқылы жұмыс жасайтын цикл жасау мүмкін емес.
E) Бір қыздырғыштан алынған жылу арқылы жасалған жұмыс жалғыз нәтижесі болатын циклы мүмкін емес. +
44. Термодинамикада энтропия қалай енгізіледі?
A) Процестердегі келтірілген жылудан алынған интеграл - энтропия күй функциясы.
B) Қайтымды процестердегі ішкі энергиядан алынған интеграл – энтропия күй функциясы.
C) Қайтымды процестердегі күй функциясының өзгерісі келтірілген жылудан алынған интеграл - энтропия. +
D) Энтропия процестің функциясы, ал оның өзгерісі келтірілген жылудан алынған интегралға тең.
E) Энтропия процестің функциясы, ал оның өзгерісі келтірілген жылу.
45. Біртекті оқшауланған жүйенің энтропиясы қалай өзгереді?
A) Оқшауланған жүйенің энтропиясы тек кемиді.
B) Кез-келген жүйенің энтропиясы артады.
C) Оқшауланған термодинамикалық жүйенің энтропиясы тек өседі. +
D) Термодинамикалық жүйенің энтропиясы тек кемиді.
E) Кез-келген термодинамикалық жүйенің энтропиясы тек артады.
46. Денелер жүйесінің энтропиясы қалай анықталады?
A) Денелер жүйесінің энтропиясы осы денелер энтропиясының айырымына тең.
B) Денелер жүйесінің энтропиясы осы денелер энтропиясының көбейтіндісіне тең.
C) Денелер жүйесінің энтропиясы осы денелер энтропиясының қатынасына тең.
D) Денелер жүйесінің энтропиясы осы денелер энтропиясының қосындысына тең. +
E) Денелер жүйесінің энтропиясы осы денелер энтропиясының қосындысының логарифіміне тең.
47. Термодинамикалық ықтималдылықтың W энтропиямен байланысы қандай?
A) S= k lnW +
B) S= -kT lnW
C) S= kT lnW
D) S= RT lnW
E) S= k/ lnW
48. Термодинамикалық тепе-теңдік қалай жазылады?
A) TdS= - dU+pdV
B) dS= -dU+pdV
C) TdS=dU+pdV +
D) TdS=dQ+pdV
E) TdS=dU- pdT
49. Энтальпия қандай өрнекпен енгізіледі?
A) H=U+pT
B) H=dU+p/V
C) H=U-pdV
D) H=U+pV +
E) H=U+pV /Q
50. Қандай тәуелсіз айнымалылармен салыстырғанда ішкі энергия термодинамикалық потенциал болады?
A) T және V айнымалыларымен салыстырғанда.
B) S және Р айнымалыларымен салыстырғанда.
C) S және V айнымалыларымен салыстырғанда. +
D) Q және V айнымалыларымен салыстырғанда.
E) T және U айнымалыларымен салыстырғанда.
51. Термодинамикада қысым ішкі энергия U арқылы қалай сипатталынады?
A) 
B) 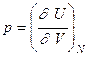
C) 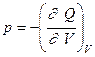
D)  +
+
E) 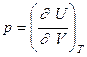
52. Қандай тәуелсіз айнымалылармен салыстырғанда энтальпия термодинамикалық потенциал болады?
Дата публикования: 2015-10-09; Прочитано: 654 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
