 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Производство этанола
|
|
Этанол С 2 Н 5 ОН – бесцветная жидкость с характерным запахом. Т кип. = 78,4 о С, Т пл. = –114,15 о С, плотность 794 кг/м3. Смешивается в любых соотношениях с водой, другими спиртами, глицерином, диэтиловым эфиром и др. растворителями. С водой, бензолом, этилацетатом, хлороформом образует азеотропные смеси. Водно-спиртовой азеотроп содержит 95,6 % об. спирта и кипит при температуре 78,1 о С. Для получения абсолютного спирта необходимо обезвоживание, например, с помощью экстракции бензолом. Этанол также образует алкоголяты с солями Са и Mg, такие как: СaСl 2  4 C 2 H 5 OH; MgCl 2
4 C 2 H 5 OH; MgCl 2  6 С 2 Н 5 ОН, что также можно использовать при обезвоживании спирта. Температура самовоспламенения спирта равна 422,8 о С, температура вспышки 13 о С, пределы взрываемости 3,28–18,95 %. Обладает наркотическим действием. ПДК составляет 1000 мл/м3 воздуха.
6 С 2 Н 5 ОН, что также можно использовать при обезвоживании спирта. Температура самовоспламенения спирта равна 422,8 о С, температура вспышки 13 о С, пределы взрываемости 3,28–18,95 %. Обладает наркотическим действием. ПДК составляет 1000 мл/м3 воздуха.
Мировое производство этанола составляет примерно 3 млн. т /год. Такая большая потребность в этаноле объясняется обширным перечнем областей его применения. При этом около половины его производства идет на получение ацетальдегида по реакции:
2СН3СН2ОН = 2СН3СНО + Н2. (14.1)
Другие области применения этанола:
- для получения диэтилового эфира
2СН3СН2ОН = СН3СН2 – О – СН2СН3 + Н2О; (14.2)
- для получения хлораля
СН3СН2ОН + 4Сl2 = CCl3 – CHO + 5HCl; (14.3)
- для получения этилацетата:

 О
О
СН3СН2ОН + СН3СООН = СН3СН2 – С – СН3; (14.4)
- для получения хлорэтила
СН3СН2ОН + НСl = CH3CH2Cl + H2O. (14.5)
Этанол используется также в качестве растворителя, в парфюмерии, медицине, а также как компонент автомобильного и авиационного топлива. Известно также его применение в производстве антифризов и тормозной жидкости на основе этиленгликоля.
Впервые этиловый спирт был получен ректификацией виноградного вина еще в 11–12 веках. Отсюда и второе его название – винный спирт. Применение спирта в медицине известно с 12 века.
В настоящее время все промышленные производства этилового спирта делятся на 4 группы и, соответственно, производят 4 сорта спирта:
- гидратация этилена (синтетический этанол);
- гидролиз древесины (гидролизный этанол);
- осахаривание крахмала (ферментативный или пищевой этанол);
- переработка сульфитных щелоков (сульфитный этанол).
Последние три способа производства этилового спирта являются биохимическими и основаны на явлении брожения углеводосодержащего сырья с образованием в качестве промежуточных продуктов сахара и/или глюкозы.
Метод гидратации этилена позволяет получить наибольший выход спирта – до 90 %. Для сравнения, выход спирта из картофеля составляет около 10 %, из зерна – 30 %, древесины – до 20 %, сульфитных щелоков – 10 %. В биохимических процессах вместе со спиртом получают такие ценные продукты, как дрожжи, фурфурол, лигнин, лигносульфонаты и даже гипс.
Впервые промышленный способ производства синтетического этилового спирта был разработан на основе метода сернокислотной гидратации этилена в две стадии в 1910–30 г.г.:
1 стадия – этерификация этилена
 OH C2H4
OH C2H4


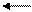
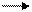 С2Н4 + Н2SO4 O2S O2S(OCH2CH3)2 (14.6)
С2Н4 + Н2SO4 O2S O2S(OCH2CH3)2 (14.6)
О – CH2CH3 диалкилсульфат
моноалкилсульфат
(этилсерная кислота)
2 стадия – гидролиз эфиров
 OH
OH
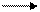 О2S – O – CH2CH3 + H2O CH3CH2OH + H2SO4; (14.7)
О2S – O – CH2CH3 + H2O CH3CH2OH + H2SO4; (14.7)
 O – CH2CH3
O – CH2CH3
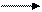
 O2S O – CH2CH3 + 2H2O 2CH3CH2OH + H2SO4. (14.8)
O2S O – CH2CH3 + 2H2O 2CH3CH2OH + H2SO4. (14.8)
В 1947 г. в США был впервые осуществлен одностадийный метод прямой гидратации этилена на твердом катализаторе, который позволил исключить из процесса агрессивную разбавленную серную кислоту и повысить выход спирта с 90 до 95 %.
Этот способ основан на реакции:
СН2 = СН2 + Н2О = СН3СН2ОН + 81 кДж /моль, (14.9)
которую сопровождают побочные:
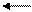
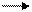 2С2Н5ОН (С2Н5)2О + Н2О; (14.10)
2С2Н5ОН (С2Н5)2О + Н2О; (14.10)
диэтиловый эфир
 nC2H4 (C2H4)n. (14.11)
nC2H4 (C2H4)n. (14.11)
полимер
Как видно из уравнения основной реакции, процесс протекает в газовой фазе с уменьшением объема и выделением тепла. Следовательно, по принципу Ле-Шателье равновесие можно сместить вправо путем снижения температуры и повышения давления и концентрации исходных веществ. Однако сни-жение температуры, как известно, приводит к падению скорости процесса.
Исследования по оптимизации параметров процесса показали, что наилучшие показатели могут быть достигнуты при давлении 5 МПа и температуре 270–275 о С и стехиометрическом соотношении реагентов. Высокую селективность при этом проявляют катализаторы ионного типа, такие как Н 3 РО 4 на диатомите или кремниевовольфрамовая кислота SiO 2 · 12 WO 3 · nH 2 O.
Так как процесс протекает в системе газ – твердое тело (катализатор), то его скорость будет определяться условиями диффузии реагентов к поверхности катализатора и адсорбционными свойствами самого катализатора, этилена и спирта. При этом этилен должен быстро адсорбироваться, а спирт десорбироваться. В этом процессе оптимальная объемная скорость подачи сырья равна 4500–5500 ч -1.
При этих условиях конверсия этилена составляет не более 5 % за один проход и поэтому процесс ведут по циркуляционной схеме (рис. 14.1).






 циркуляционный газ этанол 8 8
циркуляционный газ этанол 8 8














































































































































































































 вода катали- затор 6 вода 2 4
вода катали- затор 6 вода 2 4









 С2Н4 1 3 5
С2Н4 1 3 5





 вода 7 9 контактный газ пар
вода 7 9 контактный газ пар
вода остаток
Рис. 14.1. Технологическая схема производства этанола гидратацией этилена
1 – теплообменник; 2 – трубчатая печь; 3 – реактор; 4 – холодильник; 5 – сепаратор; 6 –промывная колонна; 7,9 – ректификационные колонны; 8 – холодильники.
Описание технологической схемы. Свежий и рециркулируемый газ сжимают до 7 МПа, смешивают между собой и с водяным паром или паровым конденсатом, нагревают в теплообменнике 1 за счет тепла реакционных газов, покидающих реактор 3. Реагенты далее подают в трубчатую печь 2, где их нагревают до 270–280 о С, а затем направляют в реактор 3, работающий в адиабатическом режиме. Реактор представляет собой контактный колонный аппарат, изготовленный из стали и облицованный внутри красной листовой медью. Реакция гидратации – слабо экзотермическая и поэтому разогрев реакционной смеси невелик. Реакционные газы после реактора охлаждают в теплообменнике 1 и подают в сборник-сепаратор 5, где происходит частичная конденсация воды и спирта. Затем парогазовая смесь проходит водяной холо-дильник 4, где конденсируются остатки спирта. Непревращенный этилен и другие газы окончательно отмывают в промывной насадочной колонне 6 и возвращают на рециркуляцию. Для поддержания постоянной концентрации этилена (80–85 %) часть газа сбрасывают в процесс продувки. Полученный раствор спирта и воды ректифицируют последовательно в колоннах 7 и 9. Го-товым продуктом является спирт-ректификат, содержащий 95,6 % спирта и 4,4 % воды. Для получения абсолютного спирта применяют азеотропную ректификацию с использованием в качестве растворителя бензола, который при кипячении с обводненным спиртом образует тройной азеотроп следующего состава, %: спирт – 18,5, бензол – 74,1, вода – 7,4, кипящий при температуре 64,9 о С. Этот азеотроп отбирают с верха колонны, а снизу выводят абсолютный спирт. На вольфрамсодержащем катализаторе конверсия этилена составляет 80 % от теоретической, а выход спирта достигает 95 % и более на превращенный этилен.
Интересны данные по себестоимости спирта, произведенного различными методами:
Синтетический спирт - 100%
Сульфитный спирт - 110%
Пшеничный спирт - 430%
Гидролизный спирт:
- из древесины - 230%
- из другого сельскохозяйственного сырья - 350%
Контрольные вопросы
1. Назовите способы производства этанола в промышленности. Где возможно, приведите химические реакции.
2. Назовите области применения этанола. Приведите химические реакции получения.
3. В чем преимущества прямой гидратации этилена по сравнению с сернокислотной при производстве этанола?
4. Какие катализаторы применяют при синтезе этанола в паровой фазе прямой гидратацией этилена.
5. Приведите параметры процесса синтеза этанола прямой гидратацией этилена.
6. Представьте технологическую схему процесса синтеза этанола прямой гидратацией этилена и опишите ее.
7. Почему для получения абсолютного спирта требуется азеотропная ректификация? Как ее осуществляют?
8. Приведите сравнительные данные по себестоимости производства этанола различными промышленными способами.
Дата публикования: 2015-10-09; Прочитано: 2319 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
