1.Составить математическое описание (систему дифференциальных уравнений) кинетики химической реакции:
| Вариант
|
|
|
|
|
|
|
|
|
|
| Реакция
| I
| II
| III
| IV
| V
| VI
| VII
| VIII
| IX
|
I.
k1 k2
  A P R A P R
 k3
S k3
S
| II.
k1 k2
  A P R A P R
 k3
S k3
S
| III.
k1 k2 k4
   A P R Q A P R Q
 k3 k5
S k3 k5
S
|
IV.
k1 k2
  A P R A P R
 k4 k3
S k4 k3
S
| V.
k1 k2 k4
   A P R Q A P R Q
 k3 k5
S k3 k5
S
| VI.
k1 k2 k4
   A P R Q A P R Q
 k3 k5
S k3 k5
S
|
VII.
k1 k2
  A P R A P R
 k3
S k3
S
| VIII.
k1 k2 k4
   A P R Q A P R Q
 k3 k5 k6
S k3 k5 k6
S
| IX.
k1 k2
  P R Q P R Q
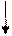 k3 k4
S k3 k4
S
|
2.Определить константу скорости реакции в случае 0, 1, 2-го порядков, если через время τ после ее начала достигнута степень превращения исходного вещества Ха. Начальная концентрация исходного вещества Са0.
| Показатель
| В А Р И А Н Т
|
|
|
|
|
|
|
|
|
|
|
|
| τ, мин
|
|
|
|
|
|
|
|
|
|
|
| Xа
| 0,6
| 0,61
| 0,62
| 0,63
| 0,64
| 0,65
| 0,66
| 0,67
| 0,68
| 0,69
|
| Са0,
кмоль/м3
| 0,21
| 0,22
| 0,23
| 0,24
| 0,25
| 0,26
| 0,27
| 0,28
| 0,29
| 0,30
|


 A P R
A P R
 k3
S
k3
S

 A P R
A P R
 k3
S
k3
S


 A P R Q
A P R Q
 k3 k5
S
k3 k5
S

 A P R
A P R
 k4 k3
S
k4 k3
S


 A P R Q
A P R Q
 k3 k5
S
k3 k5
S


 A P R Q
A P R Q
 k3 k5
S
k3 k5
S

 A P R
A P R
 k3
S
k3
S


 A P R Q
A P R Q
 k3 k5 k6
S
k3 k5 k6
S

 P R Q
P R Q
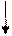 k3 k4
S
k3 k4
S