 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Различные реакции с участием СО
|
|
В реакциях СО с олефинами и алкинами участвуют также молекулы других реагентов – Н2О, ROH, RNH2 и др. Эти процессы были открыты В.Реппе в начале 40х гг XX века и протекают в растворах комплексов Ni(0, II) и Pd(0, II). Например,
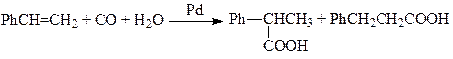 (6)
(6)
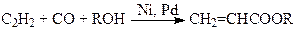 (7)
(7)
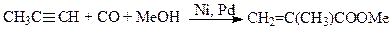 (8)
(8)
В случае олефинов активными являются гидридные комплексы палладия HPdClL, и схема механизма напоминает схему оксосинтеза
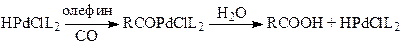 (9)
(9)
Механизм гидрокарбалкоксилирования ацетилена в растворах комплексов цис-PdBr2[P(OPh)3]2 отличается от схемы (9) – в этой системе активными комплексами являются комплексы Pd(II) (упрощенная схема):

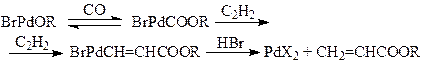
Кинетическая модель процесса (10):
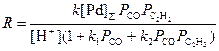 (10)
(10)
отражает образование алкоголятных комплексов палладия(II) в квазиравновесной стадии.
Процесс синтеза метилметакрилата (ММА) (8) считается в настоящее время наиболее экономически и экологически эффективным (по сравнению с ацетонциангидринным методом и окислением изобутена). Процесс разработан фирмой Shell и протекает при давлении 40 – 60 атм и температуре 110оС с очень большой скоростью (50000 моль/(моль·час)) и высокой селективностью (~100%) в растворах комплексов PdL2X2, где L – 2-PyPPh2, X – CH3SO3–, CF3SO3–, тозилат). Механизм процесса пока не ясен.
Среди новых процессов карбонилирования можно привести реакции синтеза ангидрида янтарной кислоты (11)
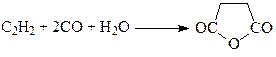 (11)
(11)
и ангидрида малеиновой кислоты (12)
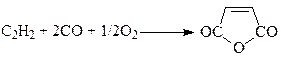 , (12)
, (12)
в которых активной формой являются комплексы Pd(I) – Pd2(CO)2Br4 (Л.Брук, О.Темкин). К промышленным процессам карбонилирования спиртов относятся процесс окислительного карбонилирования спиртов (13)
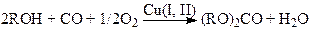 (13)
(13)
и два процесса неокислительного карбонилирования – синтез метилформиата (14) и синтез уксусной кислоты (15) по методам фирмы “Monsanto” и фирмы “Cativa”.
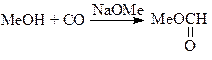 (14)
(14)
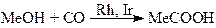 (15)
(15)
13.3. Процессы карбонилирования метанола
до уксусной кислоты
В процессе фирмы “Monsanto” активным катализатором является комплекс Rh(CO)2I2–, а в процессе фирмы “Cativa” – Ir(CO)2I2–. Основные стадии процесса в случае комплексов родия:
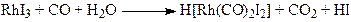 (16)
(16)
(формирование активного комплекса Rh(I))
Вторым катализатором процессе является HI.
 (17)
(17)
 (18)
(18)
 (19)
(19)
В условиях, когда концентрация воды в СН3СООН > 8% (масс) переход Rh(I) в Rh(III) в стадии (18) является медленной стадией. Распад ацильного комплекса до CH3COI и Rh(CO)2I2– или под действием Н2О (или МеОН) приводит к образованию СН3СООН
 (20)
(20)
 (21)
(21)
 (22)
(22)
Скорость реакции описывается уравнением (23)
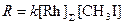 , (23)
, (23)
что свидетельствует о существовании Rh, в основном, в форме Rh(CO)2I2–. Хотя скорость не зависит от РСО, давление СО необходимо для сохранения в растворе карбонилов Rh(I). Условия процесса – РСО = 30 атм и Т = 150 – 170оС. Если содержание воды < 8%, лимитирует стадия восстановительного элиминирования (20).
В ходе процесса наблюдаются реакция конверсии СО
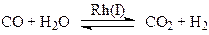 (24)
(24)
реакции образования метилацетата, диметилового эфира, этанола и пропионовой кислоты. Однако, селективность образования уксусной кислоты (на метанол) > 99%, а на СО – 90% (из-за реакции 24). Потери родия составляют 0.1г на 1 тонну кислоты, что при производительности установки 160 тыс.тонн составляет 16 кг в год.
Усовершенствование процесса при переходе к комплексам Ir (“Cativa”-процесс, BP и “Monsanto”) связано с тем, что аналогичный Rh(I) комплекс Ir [Ir(CO)2I2–] более устойчив в широком диапазоне РСО и [Н2О]. Так, комплекс устойчив при ~0.5% концентрации Н2О в отличие от комплекса Rh (> 8% H2O). Показано, что скорость присоединения CH3I к Ir(I) ~ в 150 раз выше, чем в случае Rh(I) (стадия 18), и не лимитирует процесс. Медленной стадией в этой системе считают реакцию (26) внедрения СО в метильном комплексе Ir(III), следующую за стадией замещения I– (25)
 (25)
(25)
 (26)
(26)
 (27)
(27)
Скорость процесса описывается уравнением (28)
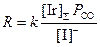 (28)
(28)
в предположении, что в быстрой квазиравновесной стадии
 (29)
(29)
равновесие практически полностью смещено вправо и весь [Ir]å @ [CH3Ir(CO)2I3–]. Производительность по СН3СООН в процессе “Cativa” ~ в 2 раза выше, чем в процессе “Monsanto” и составляет ~2кг/л·час.
Возможность использования растворов с низкой концентрацией воды в случае Ir приводит к тому, что в технологической схеме исключается колонна осушки. Это обстоятельство, вместе с более высокой производительностью и с более низкой ценой Ir (~ в 170 раз дешевле Rh) делает процесс “Cativa” более экономически эффективным.
Вопросы для самоконтроля
1) Объясните причины торможения оксидом углерода процесса оксосинтеза в случае кобальтовых и родиевых катализаторов.
2) Почему более активные олефины в случае родиевых катализаторов увеличивают срок жизни катализатора?
3) Какие процессы с участием СО связаны с именем В.Реппе?
4) Чем различаются кинетические модели процессов синтеза уксусной кислоты фирм “Monsanto” и “Cativa”? В чем причина различий в моделях?
5) Каковы достоинства технологии фирмы “Cativa”?
Литература для углубленного изучения
1. Катализ в промышленности, под ред. Б.Лича, М., Мир, 1986, т. 1, 2.
2. Шелдон Р.А., Химические продукты на основе синтез-газа, М., Химия, 1987.
3. Jones J.H., The Cativa™ Process for Manufacture of Acetic Acid, Platinum Metals Rev., 2000, 44 (3), pp. 94 – 105.
4. Темкин О.Н., Брук Л.Г., Комплексы Pd(II, I, 0) в реакциях окислительного карбонилирования, Кинетика и катализ, 2003, №5.
Дата публикования: 2015-09-18; Прочитано: 546 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
