 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задания для внеаудиторной работы
|
|
1. Что такое гомологические ряды и их значение в органической химии?
2. Что называется первичным, вторичным, третичным и четвертичным углеродными атомами?
3. Какие реакции свойственны предельным углеводородам?
4. В чем заключается правило Марковникова? Напишите уравнение реакции взаимодействия пропена с HCl.
5. Особенности окисления алкенов в нейтральной и кислой средах. Напишите уравнения реакций окисления пропена в нейтральной и кислой средах.
6. Напишите уравнения реакций присоединения водорода, хлора, хлороводорода к ацетилену. В каком случае нужно использовать правило Марковникова?
7. Напишите уравнения реакций нитрования и бромирования бензола. Укажите условия.
8. Назовите соединения в соответствии с номенклатурой ИЮПАК.
1)

| 4)
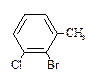
|
2)
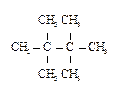
| 5)

|
3)
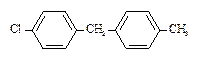
| 6)
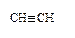
|
Лабораторная работа № 2 «Углеводороды. Химические свойства и качественный функциональный анализ»
Опыт 1.Химические свойства алканов
Отношение к окислению. В каждую из трех пробирок поместите по 1 капле любого алкана или смеси алканов (вазелиновое масло, петролейный эфир) и добавьте по 4 капле воды и 1 капле 2% перманганата калия. Затем в первую пробирку внесите 1 каплю концентрированного растворара гидроксида натрия, во вторую – 1 каплю концентрированной серной кислоты. Пробирки несколько раз энергично встряхните и отметьте, какую окраску имеет эмульсия в каждой пробирке. Содержимое каждой пробирки прокипятите в течение нескольких минут. Происходит ли при этом изменение окраски?
Вопросы:
1. Сравните действие окислителей – перманганата калия в нейтральной, кислой и щелочной средах – при комнатной температуре и при нагревании.
2. На основании проделанного эксперимента сделайте вывод об отношении алканов к окислению.
Бромирование при облучении УФ-светом. В две кварцевые кюветы поместите по 3-4 мл любого алкана или их смеси, добавьте по 4-5 капель 5% раствора брома в тетрахлорометане и перемешайте. Одну кювету накройте колпачком из черной бумаги. Поставьте обе кюветы под источник УФ-света (например, кварцевую лампу). Через 3-4 минуты облучения снимите черный колпачок и сравните окраску растворов в обеих кюветах.
Вопросы:
1. Почему для проведения бромирования алканов необходимо облучение УФ-светом?
2. Объясните, почему в закрытой черным колпачком кювете реакционная смесь не обесцвечивается?
3. Напишите схему реакции бромирования алкана. По какому механизму протекает эта реакция?
Опыт 2. Получение и химические свойства этилена
Получение. В сухую пробирку налейте 2-3 мл готовой смеси этилового спирта и концентрированной серной кислоты, бросьте несколько кусочков “кипелок” для равномерного кипения. Закройте пробирку пробкой с газоотводной трубкой и закрепите пробирку в лапке штатива под небольшим углом. Нагрейте пробирку сначала медленно, затем, усильте нагревание. Временно отставьте горелку и прекратите нагревание.
Бромирование. Во вторую пробирку поместите немного бромной воды. Опустите в нее газоотводную трубку так, чтобы конец трубки был погружен в бромную воду. Осторожно нагрейте реакционную смесь. Как только бромная вода обесцветится, уберите вторую пробирку.
Окисление. В третью пробирку поместите немного 2% раствора перманганата калия. Опустите в нее конец газоотводной трубки. Нагрейте пробирку с реакционной смесью. Обратите внимание на изменение окраски раствора в третьей пробирке.
Вопросы:
1. Напишите схемы реакций получения, бромирования и мягкого окисления этилена.
2. О чем свидетельствует наблюдаемое в опыте обесцвечивание бромной воды и раствора перманганата калия?
Опыт 3. Получение и химические свойства ацетилена
Получение. В первую пробирку поместите кусочек карбида кальция, добавьте немного капель воды. Сразу же начинается выделение газообразного ацетилена. Закройте пробирку пробкой с газоотводной трубкой и закрепите в штативе.
Бромирование. Во вторую пробирку поместите немного бромной воды и опустите в нее конец газоотводной трубки. Происходит обесцвечивание бромной воды.
Окисление. В третью пробирку поместите немного 2% раствора перманганата калия, и опустите в нее конец газоотводной трубки. Происходит обесцвечивание раствора перманганата калия.
Вопрос:
Напишите схемы реакции получения ацетилена и качественных реакций, выполненных в этом опыте.
Опыт 4. Нитрование аренов
Нитрование бензола. В сухую пробирку налейте 3 мл нитрующей смеси (H2SO4:HNO3 = 2:1). Прилейте к ней 1 мл бензола в 3 приема, хорошо перемешивая смесь после каждого прибавления. Если смесь сильно разогревается после очередного прибавления бензола и перемешивания, ее следует охладить погружением пробирки в воду. Над нитрующей смесью появляется слой нитробензола, окрашенного в желтый цвет. Вылейте содержимое пробирки в стаканчик с холодной водой, избыток кислоты при этом растворяется в воде, нитробензол же выделяется на дне стакана в виде маслянистых капель, окрашенных в слабо-желтый цвет. Нитробензол имеет запах горького миндаля.
Вопросы:
1. Напишите схему реакции получения нитробензола из бензола.
2. Объясните ориентирующее влияние нитрогруппы и напишите реакцию последующего нитрования бензола.
Опыт 5. Окисление аренов
Окисление бензола и толуола. В две пробирки налейте по 0,5 мл бензола и толуола и прибавьте к ним по 2 мл раствора перманганата калия. Встряхните смесь и отметьте, что наблюдается при этом. Затем прибавьте в каждую пробирку такой же объем 10% серной кислоты и отметьте изменение окраски в одной из пробирок.
Вопрос:
Напишите схемы реакций окисления аренов. В чем состоит отличие?
Опыт 6. Сравнение свойств алканов различного строения. Налейте в одну пробирку 0,5 мл петролейного эфира, в другую – 0,5 мл гептана. В каждую пробирку добавьте по 2-3 капли брома в тетрахлорметане.
Встряхните пробирки, опишите наблюдаемую ораску. Нагрейте обе пробирки в стаканчике с горячей водой. Опишите и объясните наблюдения (схема реакции).
Петролейный эфир – смесь алканов, содержащая алканы разветвленного строения, например, 2-метилбутан.
Опыт 7. Сравнительные свойства алканов и алкенов. Налейте в две пробирки по 0,2-0,3 мл бромной воды, в одну пробирку добавьте 0,5 мл петролейного эфира, в другую – 0,5 мл бензина. Пробирки встряхните и опишите наблюдения. Бензин содержит 2,4,4-триметилпентен-1.
Опыт 8. Влияние заместителей на реакционную способность аренов. Налейте в 2 пробирки по 0,5 мл бензола и толуола, добавьте в каждую пробирку по 2-3 капли брома в тетрахлорметане. Встряхните пробирки, опишите наблюдения и объясните их (схема реакции). Допускается кратковременный нагрев пробирок в стаканчике с горячей водой.
Подпись преподавателя: Дата:
Дата публикования: 2015-09-17; Прочитано: 945 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
