 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Идентификация катионов неорганических веществ
|
|
Для идентификации с помощью образования труднорастворимых соединений используют как групповые, так и индивидуальные осадители.
Групповой реагент NaCl осаждает ионы Ag+, Pb2+, Hg2+,
групповой реагент (NH4)2CO3 осаждает ионы Ca2+, Sr2+, Ba2+,
групповой реагент (NH4)2S осаждает ионыAl3+, Cr3+, Fe2+, Fe3+, Mn2+, Co2+, Ni2+, Zn2+.
Если присутствуют несколько катионов, то любой катион можно идентифицировать с помощью определенной (специфической) реакции, если удалить другие катионы, мешающие этой идентификации.
Ниже приводятся некоторые качественные реакции.
Обнаружение ионов железа (II) и (III)
Катион железа (III) легко обнаруживается с помощью бесцветного раствора, содержащего тиоцианат-ион NCS‾ (роданид-ион). При действии NCS‾ на раствор соли железа (III) образуется соединение кроваво-красного цвета − тиоцианат железа (III) Fе(NCS)3:
Fe3+ + 3 NCS‾ → Fe(CNS)3.
Гексацианоферрат (II) калия (жёлтая кровяная соль) также является специфическим реактивом на ион железа (III):
3K4[Fe(CN)6] + 4Fe3+ → Fe4[Fe(CN)6]3 + 12К+.
Образуется берлинская лазурь.
Гексацианоферрат (III) калия (красная кровяная соль) является специфическим реактивом на ион железа (II):
2K3[Fe(CN)6] + 3Fe2+ → Fe3[Fe(CN)6]2 + 6К+.
Образуется турнбулева синь.
Обнаружение ионов К+ и Na+
Катионы натрия и калия относятся к I аналитической группе, которая характеризуется отсутствием группового реагента, т. е. реактива, способного осаждать все катионы этой группы из их растворов.
Летучие соединения металлов окрашивают пламя горелки:
К+ в фиолетовый цвет,
Na+ в жёлтый цвет.
Обнаружение ионов ионов S-элeментов II A группы
Ион Mg2+
Групповой реагент карбонат аммония (NH4)2СОз с раствором соли магния образует белый аморфный осадок основной соли (MgOH)2CO3, растворимый в избытке NH4Cl:
2MgCl2 + 2(NH4) 2CO3 + Н2О → (MgOH) 2CO3↓+ СО2 + 4NH4Cl,
2Mg2+ + 2CO32- + Н2О → (MgOH)2CO3↓ + CO2.
Едкие щелочи и гидроксид аммония образуют с растворами солей магния белый аморфный осадок Mg(OH)2, хорошо растворимый в кислотах и растворах аммонийных солей:
Mg2+ + 2OН‾ → Mg(OH)2↓.
Растворение в кислотах:
Mg(OH)2 + 2H+ → Mg2+ + 2Н2O.
Растворение в растворах аммонийных солей:
Mg(OH)2 + 2NH4+ ↔ Mg2+ + 2NH4OH.
Ион Ва2+
Групповой реагент карбонат аммония (NН4)2СО3 осаждает катион Ва2+ из растворов его солей в виде белого аморфного постепенно кристаллизующегося осадка ВаСО3:
BaCl2 + (NH4) 2CO3 → ВаСО3↓ + 2NH4Cl,
Ва2+ + CO32‾ → ВаСО3↓.
Осадок хорошо растворим в кислотах, в том числе и слабых.
Дихромат калия К2Сг2O7 образует с раствором соли бария желтый осадок ВаСгO4, нерастворимый в уксусной кислоте, в отличие от хромата стронция (хромат кальция хорошо растворяется в воде):
2Ba2+ + Сг2O72- + Н2O → 2ВаСгO4↓ + 2H+.
Реакцию проводят при избытке CH3COONa, который реагирует с образующимися ионами Н+, смещая равновесие вправо вследствие образования малодиссоциированной уксусной кислоты:
СН3СОO‾ + Н+ → СН3СООН.
Ион Ba2+ также можно обнаружить с помощью сульфат-иона SO42‾:
Ba2+ + SO42- → BaSO4↓
Образуется творожистый белый осадок.
Ион Са2+
Групповой реагент карбонат аммония (NН4)2СО3 осаждает из растворов солей кальция аморфный белый осадок СаСО3, который при нагревании переходит в кристаллический:
CaCl2 + (NH4) 2CO3 → СаСО3↓ + 2NH4C1,
Ca2+ + CO32‾ → СаСО3↓.
Осадок легко растворяется в минеральных и уксусной кислотах.
Оксалат аммония (NH4)2C2O4 образует с раствором соли кальция белый кристаллический осадок, растворимый в соляной, но не растворимый в уксусной кислоте:
CaCl2 + (NH4)2C2O4 → СаС2O4↓ + 2NH4C1,
Ca2+ + С2O42‾ → СаС2O4↓.
Аналогичный осадок дают ионы Ва2+ и Sr2+. Поэтому этой реакцией можно обнаружить Са2+ только при отсутствии ионов бария и стронция.
Ион Sr2+
Групповой реагент карбонат аммония (NН4)2СО3 осаждает карбонат стронция белого цвета, растворимый в уксусной, соляной и азотной кислотах:
SrCl2 + (NH4)2CO3 → SrCO3↓ + 2NH4C1.
Насыщенный раствор гипса CaSO4 . 2H2O (гипсовая вода) образует с ионами Sr2+ белый осадок сульфата стронция:
Sr2+ + SO42‾ → SrSO4↓.
Однако при действии гипсовой воды ион стронция дает не обильный осадок, а только помутнение, появляющееся не сразу из-за образования пересыщенного раствора. Появление осадка ускоряют нагреванием.
Реакция служит для обнаружения Sr2+ только при отсутствии Ba2+, которой с гипсовой водой вызывает помутнение, появляющееся сразу, так как растворимость BaSO4 меньше растворимости SrSO4 (Ks0(BaSO4) = 1,1 . 10-10, Ks0(SrSO4) = 2,8 . 10-7).
Гипсовая вода не образует осадков с растворами солей кальция ни на холоду, ни при нагревании. Этим ион Ca2+ отличается от ионов Ba2+ и Sr2+.
Ион NH4+
Влажная лакмусовая бумажка в растворе аммиака становится синей, потому что водный раствор аммиака – слабое основание, фенолфталеин подтверждает это - становится малиновым. Стеклянная палочка, смоченная в концентрированной соляной кислоте, при внесении в атмосферу аммиака вызывает появление густого белого дыма, вызванного выделением хлорида аммония
NH3 + HCl → NH4Cl.
Качественные реакции на рассмотренные выше и некоторые другие катионы представлены в табл. 6.1.
Таблица 6.1
Качественные реакции на некоторые катионы
| Катион | Воздействие или реактив | Наблюдаемая реакция |
| Li+ | Пламя | Карминово-красное окрашивание |
| Na+ | Пламя | Жёлтое окрашивание |
| K+ | Пламя | Фиолетовое окрашивание |
| Са2+ | Пламя | Кирпично-красное окрашивание |
| (NН4)2СО3 | CaCl2 + (NH4) 2CO3 → СаСО3↓ + 2NH4C1 осадок белого цвета | |
| (NH4)2C2O4 | CaCl2 + (NH4)2C2O4 → СаС2O4↓ + 2NH4C1 осадок белого цвета | |
| Mg2+ | (NН4)2СО3 | 2MgCl2 + 2(NH4) 2CO3 + Н2О → (MgOH) 2CO3↓+ СО2 + 4NH4Cl белый аморфный осадок, растворимый в избытке NH4Cl |
| NaOH | Mg2+ + 2OН‾ → Mg(OH)2↓ белый аморфный осадок | |
| Sr2+ | Пламя | Карминово-красное окрашивание |
| (NН4)2СО3 | SrCl2 + (NH4)2CO3→ = SrCO3↓ + 2NH4C1 белый осадок, растворимый в уксусной кислоте | |
| CaSO4 . 2H2O | Sr2+ + SO42-→ SrSO4↓ белый осадок | |
| Ва2+ | Пламя | Жёлто-зелёное окрашивание |
| SO42‾ | Ва2+ + S042‾ → BaS04 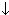 белый творожистый осадок, не растворимый в кислотах
белый творожистый осадок, не растворимый в кислотах
| |
| Cu2+ | Вода | Гидратированные ионы Cu2+ имеют голубую окраску |
| NH4OH | Cu2+ + 4 NH4OH → [Cu(NH3)4]2+ + 4H2O ярко-синее окрашивание | |
| Pb2+ | S2‾ | Pb2+ + S2‾ → PbS↓ осадок чёрного цвета |
| J‾ | Pb2+ + J‾ → PbJ2↓ осадок жёлтого цвета | |
| Ag+ | Аg+ + Cl‾ → AgCl 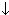 белый осадок нерастворимый в HNO3, но растворимый в контентрированном растроре аммиака
белый осадок нерастворимый в HNO3, но растворимый в контентрированном растроре аммиака
|
Продолжение табл. 6.1
| Fe2+ | K3[Fe(CN)6] | 2K3[Fe(CN)6] + 3Fe2+ → Fe3[Fe(CN)6]2 + 6К+ осадок турнбулевой сини |
| Fe3+ | K4[Fe(CN)6] | 3K4[Fe(CN)6] + 4Fe3+ → Fe4[Fe(CN)6]3 + 12К+ осадок берлинской лазури |
| КNCS | Fe3+ + 3 NCS‾ → Fe(CNS)3 кроваво-красное окрашивание | |
| Al3+ | Щёлочь | Выпадение осадка гидроксида алюминия при приливании первых порций щелочи и его растворение при дальнейшем приливании |
| NH4+ | Щёлочь, нагрев | t 0
NH4+ + ОН‾ → NH3 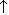 + Н20
запах аммиака + Н20
запах аммиака
|
| H+ кислая среда | Индикаторы: лакмус, метилоранж | Красное окрашивание |
Специфические реакции на некоторые анионы представлены в табл. 6.2
Таблица 6.2
Специфические реакции на некоторые анионы
| Анион | Реактив | Наблюдаемая реакция |
| S042‾ | Ва2+ | Ва2+ + S042 ‾ → BaS04 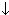 выпадение белого осадка, нерастворимого в кислотах
выпадение белого осадка, нерастворимого в кислотах
|
| N03‾ | Концентрированная H2SO4 и Сu, нагревание смеси | Образование голубого раствора, содержащего ионы Сu2+, выделение газа бурого цвета (NO2) |
| H2S04 +FeSO4 | Возникновение окраски от фиолетовой до коричневой (реакция «бурого кольца») сульфата нитрозо-железа (II) [Fe(H20)5NO]2+ | |
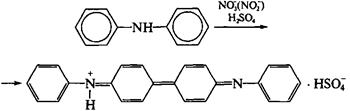
| Раствор дифениламина в концентрированной серной кислоте |
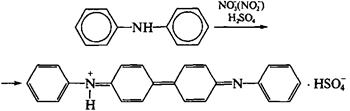 вещество интенсивного синего цвета
вещество интенсивного синего цвета
| |
| РО43‾ | Ag+ | ЗАg+ + Р043‾ → Аg3Р04 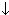 осадок светло-жёлтого цвета
осадок светло-жёлтого цвета
|
| смесь MgCI2, NH4CI и NH4OH (магнезиальная смесь) | HPO42‾ + Mg2+ + NH4OH → MgNH4PO4↓ + H2O белый кристаллический осадок, растворимый в HCI и CH3COOH, но не растворимый в аммиаке | |
| СrO42‾ | Ва2+ | Ва2+ + СrO42‾ → BaCr04 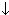 желтый осадок, не растворимый в уксусной кислоте, но растворимый в HCI
желтый осадок, не растворимый в уксусной кислоте, но растворимый в HCI
|
| S2‾ | Рb2+ | Pb2+ + S2‾ → PbS 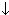 черный осадок
черный осадок
|
Продолжение табл. 6.2
| СО32‾ | Са2+ | Са2+ + С032‾ → СаСОз 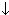 белый осадок, растворимый в кислотах
белый осадок, растворимый в кислотах
|
| Н+ (сильная кислота) | СО32‾ + 2Н+ → Н2О + СО2↑ выделение углекислого газа | |
| SO32‾ | Н+ | 2Н+ + SO32‾ → Н20 + S02↑ характерный запах S02 |
| F‾ | Са2+ | Са2+ + 2F‾ →CaF2↓ белый осадок |
| Cl‾ | Аg+ | Аg+ + Cl‾ → AgCl 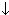 белый осадок нерастворимый в HNO3, но растворимый в контентрированном растроре аммиака
белый осадок нерастворимый в HNO3, но растворимый в контентрированном растроре аммиака
|
| Br‾ | Аg+ | Ag+ + Br‾ = AgBr 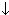 светло-жёлтый осадок нерастворимый в HNO3,темнеет на свету
светло-жёлтый осадок нерастворимый в HNO3,темнеет на свету
|
| J‾ | Аg+ | Аg+ + J‾  АgJ АgJ 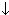 жёлтый осадок нерастворимый в HNO3 и концентрированном NH3, темнеет на свету
жёлтый осадок нерастворимый в HNO3 и концентрированном NH3, темнеет на свету
|
| ОН‾ (щелочная среда) | индикаторы: лакмус фенолфталеин | синее окрашивание малиновое окрашивание |
Пример 1. Для обнаружения в растворе катионов кальция используют …
1) нитрат аммония 2) сульфид аммония 3) оксалат аммония 4) хлорид аммония
Решение: Для обнаружения в растворе катионов кальция используют оксалат аммония:
CaCl2 + (NH4)2C2O4 = СаС2O4↓ + 2NH4C1,
Ca2+ + С2O42- = СаС2O4↓.
Пример 2. Присутствие нитрат-ионов в растворе можно доказать, используя в качестве реактива …
1) магнезиальную смесь 2) дифениламин 3) раствор щелочи 4) раствор иода
Решение.
Добавление нескольких капель раствора дифениламина в концентрированной серной кислоте к раствору, содержащему нитрат-ионы, приведет к появлению синей окраски раствора:
NO3– + дифениламин  вещество интенсивного синего цвета
вещество интенсивного синего цвета
Дата публикования: 2015-07-22; Прочитано: 3605 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
