 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Часть 2. Ионообменная хроматография
|
|
Лабораторная работа №6
Применение хроматографических методов при определении аминокислотного состава белков
Часть 2. Ионообменная хроматография
Ионообменная хроматография - жидкостная хроматография. основанная на различной способности разделяемых ионов к обмену с фиксированных ионами сорбента (неподвижная фаза), образующимися в результате диссоциации ионогенных групп последнего. В качестве сорбента в аналитических целях наибольшее распространение получили синтетические ионообменные смолы.
Ионообменная смола представляет собой трехмерную решетку высокополимера, чаще всего полистирола, к которому привиты функциональные группировки, ионизированные или ионизируемые и определяющие свойства ионообменных смол.
Различают два вида ионообменников по знаку заряда функциональных группировок:
а) катиониты: сульфо- 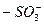 , карбоксильные-
, карбоксильные-  , аминодиацетатные-
, аминодиацетатные- 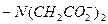 , фосфорнокислые-
, фосфорнокислые- 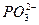 и т.д.;
и т.д.;
б) аниониты: четвертичные аммониевые соединения 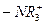 , третичные
, третичные  , фосфониевые
, фосфониевые  , сульфониевые
, сульфониевые 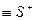 и т.д.
и т.д.
В сухом состоянии смолы группы а) представлены в кислых формах или в виде их солей. Смолы группы б) – в виде свободных оснований (третичные амины), или гидроокисей (четвертичные аммониевые соединения) или в виде их солей.
В зависимости от степени диссоциации привитых функциональных групп на ионы различают сильнокислотные и сильноосновные (функциональные группы диссоциированы полностью), а также слабокислотные и слабоосновные (частичная диссоциация функциональных групп). Использование ионообменных смол второй группой зависит от рН растворов.
Используемая при разделении компонентов смеси подвижная фаза (растворитель или смесь растворителей) носит название элюента; вытекающий из хроматографической колонки раствор – элюата.
Очистка глицина от неорганических солей с помощью ионообменной хроматографии
Колонку заполняют предварительно подготовленным катионитом (избегая образования в слое смолы пузырьков воздуха, а также следя за тем, чтобы катионит был полностью покрыт жидкостью) и обрабатывают 2-3-кратным объемом 1 н раствором соляной кислоты, а затем дистиллированной водой до нейтральной реакции вытекающего раствора по метиловому оранжевому. Высота слоя катионита должна составлять 15-20 см.
Через колонку с катионитом пропускают 10 мл раствора глицина, содержащего примесь хлорида бария со скоростью не более 10 капель в минуту. При этом происходит поглощение как ионов Ba2+, так и глицина. Затем с той же скоростью промывают катионит дистиллированной водой до тех пор, пока в элюате не исчезнет кислая реакция среды. Полученные растворы объединяют в колбу для титрования. Суммарное уравнение данного процесса выглядит следующим образом:
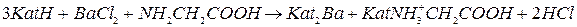
Для определения количества хлорида бария, содержащегося в смеси, раствор титруют 0,01 н раствором гидроксида натрия до синей окраски индикатора.
Массовую концентрацию в г/л BaCl2 (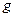 ), находившегося в смеси с глицином, определяют по формуле:
), находившегося в смеси с глицином, определяют по формуле:
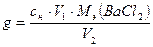
где 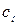 - нормальная концентрация раствора NaOH, моль/л;
- нормальная концентрация раствора NaOH, моль/л;
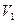 - объем раствора NaOH, пошедшего на титрование элюата, мл;
- объем раствора NaOH, пошедшего на титрование элюата, мл;
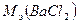 - молярная масса эквивалента хлорида бария, г/моль;
- молярная масса эквивалента хлорида бария, г/моль;
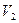 - объем исходного раствора глицина с примесью хлорида бария, мл.
- объем исходного раствора глицина с примесью хлорида бария, мл.
Для вытеснения глицина из катионита колонку промывают 2%-м водным раствором аммиака, пропуская его с той же скоростью. Вытекающий из колонки раствор собирают в отдельные приемники объемом по 5 мл до появления щелочной реакции. Суммарное уравнение:
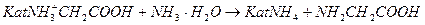
Нейтральные фракции элюата объединяют, отбирают 1 мл раствора и проводят пробу на ионы Ba2+. Оставшийся раствор выпаривают в фарфоровой чашке на водяной бане с получением глицина, свободного от неорганических примесей. Оценку качественного состава полученного препарата проводят методом распределительной хроматографии на бумаге.
По окончании опыта проводят регенерацию катионообменой смолы. Для этого пропускают через колонку 2-3-кратный объем 1 н раствора соляной кислоты и затем дистиллированную воду до нейтральной реакции среды.
Разделение смеси аминокислот на ионообменных смолах
Разделение смеси аминокислот методом ионообменной хроматографии основано на различии в их изоэлектрических точка. Аминокислоты можно условно разделить на три группы: основные, нейтральные и кислые. К первым относятся диаминомонокарбоновые кислоты с изоэлектрической точкой, лежащей при 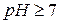 . Нейтральные аминокислоты представляют собой моноаминомонокарбоновые кислоты с изоэлектрической точкой, лежащей в пределах
. Нейтральные аминокислоты представляют собой моноаминомонокарбоновые кислоты с изоэлектрической точкой, лежащей в пределах 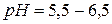 . Наконец, кислые аминокислоты являются моноаминодикарбоновыми кислотами. Их изоэлектрическая точка находится при
. Наконец, кислые аминокислоты являются моноаминодикарбоновыми кислотами. Их изоэлектрическая точка находится при 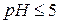 . Таким образом, в зависимости от рН среды поведение различных групп аминокислот будет различным, их ионы будут обладать разным знаком и числом зарядов. Это свойство и позволяет применять ионообменники для разделения смеси аминокислот.
. Таким образом, в зависимости от рН среды поведение различных групп аминокислот будет различным, их ионы будут обладать разным знаком и числом зарядов. Это свойство и позволяет применять ионообменники для разделения смеси аминокислот.
Успех разделения зависит от правильного выбора рН среды, а также соответствующей формы ионообменника.
Разделение смеси глицина (pI=5,97) и глутаминовой кислоты (pI=3,22)
Хроматографическую колонку заполняют набухшим анионитом (избегая образования в слое смолы пузырьков воздуха, а также следя за тем, чтобы анионит был полностью покрыт жидкостью) и обрабатывают 2-3-кратным объемом 1 н раствора соляной кислоты, а затем дистиллированной водой до отрицательной реакции на ионы Cl-. Высота слоя анионита должна составлять 15-20 см. Затем через колонку пропускают около 25 мл 0,001 н раствора соляной кислоты (рН =3), после чего вносят 5 мл смеси исследуемых аминокислот, значение рН которой должно быть приблизительно равным четырем. При таком условии глутаминовая кислота, обладая отрицательным зарядом, хорошо обменивается с ионами анионита. При 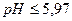 глицин находится в катионной форме и не задерживается в процессе разделения.
глицин находится в катионной форме и не задерживается в процессе разделения.
Затем колонку с анионитом промывают раствором соляной кислоты с 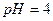 до отрицательной реакции на нингидрин в отдельных пробах элюата объемом по 5 мл. Для проведения качественной реакции несколько капель исследуемого раствора наносят на фильтровальную бумагу, пятно обводят простым карандашом, подсушивают над песчаной баней или плиткой, с помощью пульверизатора обрабатывают раствором нингидрина в ацетоне и вновь выдерживают при нагревании (в случае присутствия в пробе аминокислоты появляется характерная окраска).
до отрицательной реакции на нингидрин в отдельных пробах элюата объемом по 5 мл. Для проведения качественной реакции несколько капель исследуемого раствора наносят на фильтровальную бумагу, пятно обводят простым карандашом, подсушивают над песчаной баней или плиткой, с помощью пульверизатора обрабатывают раствором нингидрина в ацетоне и вновь выдерживают при нагревании (в случае присутствия в пробе аминокислоты появляется характерная окраска).
Вытеснение сорбированных аминокислот проводят 1 н раствором соляной кислоты. Элюат собирают в отдельные приемники по 5 мл. Вымывание прекращают также после получение отрицательной реакции на нингидрин.
На каком этапе происходит выделение аминоуксусной и глутаминовой кислот?
По окончании опыта проводят регенерацию анионообменой смолы. Для этого пропускают через колонку 2-3-кратный объем 1 н раствора соляной кислоты и затем дистиллированную воду до отрицательной реакции на хлорид-ионы.
Дата публикования: 2015-07-22; Прочитано: 777 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
