 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Введение. Поверхностное натяжение – это характеристика поверхности раздела двух фаз, находящихся в равновесии
|
|
Поверхностное натяжение – это характеристика поверхности раздела двух фаз, находящихся в равновесии. Поверхностное натяжение имеет место на границах твердое тело-жидкость, жидкость-газ, жидкость-жидкость, твердое тело-газ. Рассмотрим механизм возникновения поверхностного натяжения. Молекула внутри вещества (1) окружена такими же молекулами со всех сторон, а молекула, находящаяся на поверхности (2), окружена «своими» молекулами только с одной стороны, а с другой находятся молекулы другой фазы (рис.1). При таком условии молекулярные силы, действующие на молекулу (2), оказываются неуравновешенными, их равнодействующая R направлена вглубь жидкости перпендикулярно к её поверхности.

Рис.1. Механизм возникновения поверхностного натяжения
Таким образом, молекулы на поверхности обладают дополнительной
потенциальной энергией по сравнению с молекулами в объеме, т.е. поверхностной энергией. Величина этой энергии пропорциональна площади поверхности. Чтобы создать поверхность раздела фаз площади S, необходимо совершить работу, равную
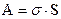 (1)
(1)
где 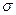 - коэффициент пропорциональности или коэффициент поверхностного натяжения.
- коэффициент пропорциональности или коэффициент поверхностного натяжения.
Поверхностное натяжение измеряется в 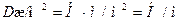 . В старой системе
. В старой системе  ,
, 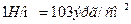 .
.
Таким образом, коэффициент поверхностного натяжения численно равен работе, необходимой для увеличения площади поверхности при постоянной температуре и давлении на единицу. Коэффициент поверхностного натяжения
зависит от вида контактирующих фаз, концентрации, температуры и т.д.
С увеличением температуры величина поверхностного натяжения уменьшается и становится нулем при увеличении температуры до критической (Критическая температура - эта та температура, начиная с которой ни при каком давлении нельзя превратить газ в жидкость. Для воды это 374Со).
Наиболее известная эмпирическая зависимость поверхностного натяжения от температуры была предложена Лорандом Этвёшом, так называемое правило Этвёша.
Зависимость коэффициента поверхностного натяжения от концентрации раствора определяется по эмпирическому уравнению Б.А.Шишковского:
 (2)
(2)
где: 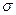 - поверхностное натяжение растворителя (воды);
- поверхностное натяжение растворителя (воды);
 - поверхностное натяжение растворенного вещества (ПАВ);
- поверхностное натяжение растворенного вещества (ПАВ);
С – концентрация раствора, моль/л;
В – константа;
К – удельная капиллярная постоянная.
Поверхностное натяжение является причиной капиллярных явлений, явлений смачивания и не смачивания, оно является важным фактором многих технологических процессов. Например, для извлечения минералов из руды используют флотацию (продувание воздуха через суспензию руды).
Дата публикования: 2015-07-22; Прочитано: 577 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
