 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Ферменты желудка
|
|
Пепсиногеннеактивный фермент, Пепсин гидролизует внутренние пептидные связи в белке с образованием коротких пептидов:хорошо - между ароматическими аминокислотами (фенилаланин, триптофан, тирозин) и хуже -между лейцином и дикарбоновыми аминокислотами.
Гастриксин – эндопептидаза,. Образуется из пепсиногена, гидролизует внутренние пептидные связи в белке с образованием коротких пептидов.
Муцин – мукопротеид образующий слизь. Существует в 2 формах: нерастворимая фракция - покрывает поверхность слизистой оболочки и изолирует эпителий от пищеварительного процесса (механическая и химическая защита); растворимая фракция - образует коллоидную систему, в которой растворены компоненты желудочного сока. Обладает буферными свойствами, способна нейтрализовать кислотность или щелочность.
Фактор Касла– гастромукопротеид, содержит пептид, отщепляющийся оп пепсиногена (секрет главных клеток) и мукоид (секрет добавочных клеток). Или образуется париетальными клетками?.Фактор Касла связывает «внешний фактор» – витамин В12, предотвращает его разрушение и способствует всасыванию.
Лизоцим - белок, обеспечивающий бактерицидные свойства желудочного сока.



Ферменты кишечнка обладают специфичностью к определенным а.к: трипсин гидролизует пептидные связи, образрванные карбоксильным группами катионогенных аминокислот арг и лиз.; химотрипсин -пептидные св.ароматич.а.к.фен, тир, три; эластаза- связи гли и ала; карбоксипептидаза отщепляет С-концевые а.к; аминопептидаза отщ. N-концевые а.к.; дипептидаза -гидролизует дипептиды из 2х любых а.к.; трипептидаза -трипептиды.;
4. Гниение – превращения аминокислот, вызванные деятельностью микроорганизмов в толстом кишечнике. Усилению процессов гниения аминокислот могут способствовать:избыточное поступление белков с пищей; врождённые и приобретённые нарушения процесса всасывания аминокислот в кишечнике; снижение моторной функции кишечника.
В результате гниения аминокислот образуются различные вещества, многие из которых являются токсичными для организма
Продукты гниения аминокислот являются ксенобиотиками – веществами, чужеродными для организма человека и должны быть обезврежены (инактивированы).
Обезвреживание продуктов гниения аминокислот происходит в клетках печени после поступления веществ из кишечника с кровью воротной вены. Продукты обезвреживания хорошо растворяются в воде и поэтому легко выводятся из организма. Процесс обезвреживания включает, как правило, две фазы (стадии): фазу модификации и фазу конъюгации. В фазе модификации вещества вступают в реакции микросомального окисления, в результате которого образуются полярные группы —ОН или —СООН. Если такие группы уже имеются, то обезвреживание может происходить непосредственно путём конъюгации. Реакции конъюгации заключаются в том, что к указанным группам присоединяется определённое соединение (глюкуроновая кислота, серная кислота, глицин и некоторые другие). Активной формой глюкуроновой кислоты является уридиндифосфоглюкуроновая кислота (УДФГК), активной формой серной кислоты - 3'-фосфоаденозин-5'-фосфосульфат (ФАФС).
5.
6.Под т рансаминированием подразумевают реакции межмолекулярного переноса аминогруппы (NH2—) от аминокислоты на α-кетокислоту без промежуточного образования аммиака. Биологическое значение: 1. ОБЕСПЕЧИВАЮТ СИНТЕЗ НОВЫХ АМИНОКИСЛОТ ИЗ ЧИСЛА ЗАМЕНИМЫХ. Из заменимых аминокислот также могут образоваться необходимые клетке кетокислоты. При избытке какой-либо из кислот соотношение быстро восстанавливается трансаминазой за счет другой пары. Недостающее количество какой-либо из кислот может быть взято клеткой из других метаболических путей (например, альфа-кетоглутарат может быть взят из ЦТК). Избыток какой-либо из кислот может быть ликвидирован другими ферментами (например, избыточное количество глутамата окисляется глутаматдегидрогеназой).
2. ОБЕСПЕЧИВАЮТ ПРОТЕКАНИЕ РЕАКЦИЙ КОСВЕННОГО ДЕЗАМИНИРОВАНИЯ.
3. ОБЕСПЕЧИВАЮТ СИНТЕЗ МОЧЕВИНЫ
Главные особенности реакции трансаминирования:
1. Это циклический процесс, все стадии которого катализируются одним и тем же ферментом - трансаминазой данной пары кислот. В этот цикл вступает одна аминокислота и кетокислота (в приведенном примере - это глутамат и ПВК). Образуются другая альфа-кетокислота и аминокислота (в приведенном примере - альфа-кетоглутарат и аланин).
2. Все стадии этого процесса обратимы. Поэтому весь цикл в целом может протекать как в прямом, так и в обратном направлении. Направление этого цикла зависит от соотношения концентраций участников реакции - всех четырех кислот. Резко повысив концентрацию какой-либо одной из кислот, можно направить реакцию по определенному направлению.
3. Каждая трансаминаза обычно специфична для одной пары субстратов и соответствующей ей пары продуктов и все стадии реакции катализируются только одним ферментом. По участникам процесса для данного фермента дают ему название:
Фермент, который катализирует приведенную реакцию, можно назвать: Аланинаминотрансфераза (АлТ) (глутаминово-пировиноградная трансаминаза (ГПТ)).4. Трансаминазы обычно обладают высокой субстратной специфичностью и высокой активностью. Наиболее активными в клетках являются те трансаминазы, для которых хотя бы один из субстратов является дикарбоновой альфа-кетокислотой - это АлТ - аланинаминотрансфераза (ГПТ) и АсТ - аспартатаминотрансфераза (ГЩТ).Определение активности этих ферментов в сыворотке крови имеет важное значение в дифференциальной диагностике таких заболеваний, как вирусный гепатит и инфаркт миокарда.
АсТ и АлТ являются внутриклеточными ферментами. Поэтому в норме их активность в крови очень мала. При вирусном гепатите или при инфаркте миокарда наблюдается разрушение клеток печени или миокарда соответственно. Поэтому в крови будет наблюдаться повышение активности и АлТ, и АсТ, но неодинаковое для каждого из ферментов.
В клетках сердечной мышцы (миокарда) содержится гораздо больше АсТ, чем АлТ, а в клетках печени - наоборот: АлТ намного больше, чем АсТ. Поэтому при инфаркте миокарда активность АСТ в крови будет значительно выше, чем АЛТ, а при вирусном гепатите активность АЛТ будет выше, чем АСТ.Поэтому определение активности этих ферментов в крови помогает врачам в постановке правильного диагноза.
10.источники аммиака в клетке. Катаболизм аминокислот в тканях происходит постоянно со скоростью ∼100 г/сут. При 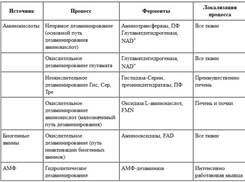 этом в результате дезаминирования аминокислот освобождается большое количество аммиака. начительно меньшие количества его образуются при дезаминировании биогенных аминов и нуклеотидов. Основные источники аммиака в клетках представлены в табл. 9-3.
этом в результате дезаминирования аминокислот освобождается большое количество аммиака. начительно меньшие количества его образуются при дезаминировании биогенных аминов и нуклеотидов. Основные источники аммиака в клетках представлены в табл. 9-3.
Часть аммиака образуется в кишечнике в результате действия бактерий на пищевые белки (гниение белков в кишечнике) и поступает в кровь воротной вены. Концентрация аммиака в крови воротной вены существенно больше, чем в общем кровотоке. В печени задерживается большое количество аммиака, что поддерживает низкое содержание его в крови. Концентрация аммиака в крови в норме редко превышает 0,4-0,7 мг/л (или 25-40 мкмоль/л). В крови и цитозоле клеток при физиологических значениях рН аммиак переходит в ион аммония - NH4+, количество неионизированного NH3 невелико (~1%)
. 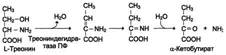
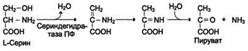
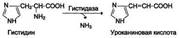
Аммиак, образующийся в тканях, сначала превращается в нетоксичное соединение и в таком виде переносится кровью к печени или почкам. Такими транспортными формами являются аминокислоты глутамин, аспарагин и аланин.
. Образование глутамина и аспарагина из глутамата и аспартата соответственно происходит во многих тканях, включая головной мозг:
Глутамин - нейтральное нетоксичное соединение, способное легко проходить через клеточные мембраны. В виде этой аминокислоты аммиак транспортируется в крови. В крови здоровых людей содержание глутамина существенно превышает содержание других аминокислот. Глутамин, помимо участия в синтезе белка, служит источником азота в биосинтезе гистидина, глюкозамина, пуриновых и пиримидиновых нуклеотидов. С кровью глутамин поступает в печень и почки. Здесь он под действием фермента глутаминазы превращается в глутамат и аммиак. При участии аспарагиназы также происходит образование аммиака из аспарагина.
. Аланин является транспортной формой аммиака, которая образуется преимущественно в мышцах. При интенсивной физической нагрузке источниками аммиака служат реакции дезаминирования аминокислот и аденозинмонофосфата (АМФ). Сначала аммиак превращается в аминогруппу глутамата в реакции восстановительного аминирования, катализируемой глутаматдегидрогеназой(см. параграф 18.6.2):
Образовавшийся глутамат переносит затем свою α-аминогруппу на пируват, всегда имеющийся в достаточном количестве, поскольку это продукт протекающего в мышцах гликолиза. Реакция катализируется аланинаминотрансферазой.
Глутамат + Пируват α-Кетоглутарат + Аланин
Аланин (нейтральная аминокислота, не несущая суммарного заряда при значениях рН, близких к 7) выходит из клеток и доставляется кровью к печени. Здесь он под действием аланинаминотрансферазы передаёт свою аминогруппу α-кетоглутарату, в результате чего образуется глутамат.
α-Кетоглутарат + Аланин Глутамат + Пируват
Далее в реакции, катализируемой глутаматдегидрогеназой, глутамат дезаминируется с образованием α-кетоглутарата и аммиака, который в печени превращается в мочевину.
11.
Дата публикования: 2015-07-22; Прочитано: 353 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
