 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
I. Химическое равновесие
|
|
1.1. ОСНОВНЫЕ ПОНЯТИЯ
Большинство химических реакций являются обратимыми:
- Обратимыми называются химические реакции, которые одновременно протекают и в прямом, и в обратном направлениях.
Уравнение обратимой реакции записывается
nA×A(г) + nB×B(г) D nD×D(г) + nF×F(г) (1)
→ прямое направление реакции;
← обратное направление реакции.
Закон действующих масс для прямого и обратного направлений записывается:
 ,
,
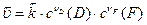 .
.
В ходе обратимой химической реакции концентрации реагентов уменьшаются, концентрации продуктов увеличиваются и, соответственно, уменьшается скорость прямой реакции и увеличивается скорость обратной. Наступает момент, когда они становятся равными. Это состояние обратимой реакции называется химическим равновесием.
Химическое равновесие – состояние обратимой реакции, характеризующееся равенством скоростей прямой и обратной реакций при постоянных значениях параметров процесса (температуре, давлении, объеме системы и концентрации веществ).
Кинетическое условие равновесия:
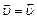 (2)
(2)
Химическое равновесие является динамическим, поскольку и прямая, и обратная реакции в состоянии равновесия продолжают протекать, но с одинаковыми скоростями.
Концентрации участников реакции, которые устанавливаются в момент равновесия, называются равновесными и обозначаются: [A], [B], [F], [D], моль/л.
Скорости прямого и обратного процессов в момент равновесия равны соответственно:
 , ,
| (3) |
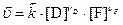 . .
|
Равновесные концентрации связаны с начальными (исходными) концентрациями веществ (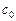 ) соотношениями:
) соотношениями:
| для реагентов: | для продуктов | |

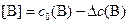
| 

| (4) |
Чаще всего концентрации продуктов реакции в начальный момент равны нулю:  ;
;  , в этом случае
, в этом случае
[D] = Dc(D),
[F] = Dc(F).
Изменения концентраций (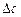 ) веществ, участвующих в реакции, пропорциональны стехиометрическим коэффициентам.
) веществ, участвующих в реакции, пропорциональны стехиометрическим коэффициентам.
 = const (5)
= const (5)
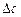 реагентов показывает, сколько прореагировало данного вещества,
реагентов показывает, сколько прореагировало данного вещества, 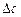 продуктов – сколько вещества образовалось к моменту наступления равновесия.
продуктов – сколько вещества образовалось к моменту наступления равновесия.
1.2. РАСЧЕТ КОНСТАНТЫ ХИМИЧЕСКОГО РАВНОВЕСИЯ
Количественной характеристикой или законом действующих масс для обратимых химических реакций является константа химического равновесия (Kc).
Для гомогенной химической реакции (1) она запишется:
 (6)
(6)
Например, для реакции:
2NO(г) + Cl2(г) D NOCl(г),
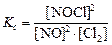 . (7)
. (7)
В гетерогенных химических процессах конденсированные фазы (тв, ж) не учитываются при записи и расчете  .
.
Например, для реакции:
TiO2(тв) + 2C(тв) + 2Cl2(г) D TiCl4(г) + 2CO(г)
 . (8)
. (8)
Константа равновесия зависит только от природы веществ и температуры и не зависит от концентрации веществ и присутствия катализатора.
Константа равновесия указывает на глубину протекания процесса. Если 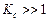 , это значит, что равновесные концентрации продуктов реакции F и D больше, чем равновесные концентрации реагентов A и B. Если
, это значит, что равновесные концентрации продуктов реакции F и D больше, чем равновесные концентрации реагентов A и B. Если  , равновесие устанавливается при больших концентрациях реагентов A и B и малых концентрациях продуктов F и D,.
, равновесие устанавливается при больших концентрациях реагентов A и B и малых концентрациях продуктов F и D,.
Расчет  сводится к определению равновесных концентраций участвующих в реакции веществ.
сводится к определению равновесных концентраций участвующих в реакции веществ.
Пример 1. Рассчитайте  реакции
реакции
2SO2(г) + O2(г) D 2SO3(г),
если исходные концентрации 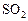 и
и  равны соответственно 0,4 и 0,3 моль/л, а к моменту равновесия образовалось 0,2 моль/л оксида серы (VI).
равны соответственно 0,4 и 0,3 моль/л, а к моменту равновесия образовалось 0,2 моль/л оксида серы (VI).
Решение.
Реакция гомогенная, поэтому
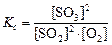 .
.
Для удобства и наглядности внесем условия задачи в таблицу:
Таблица 1
   D D 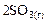
| |||
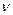
| |||
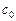 , моль/л , моль/л
| 0,4 | 0,3 | |
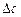 , моль/л , моль/л
| |||
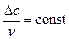
| |||
| [В], моль/л | 0,2 |
Далее, по мере расчета определяемых величин будем вносить их значения в таблицу.
В соответствии с (4) запишем выражения равновесных концентраций для всех веществ:
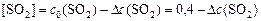

 = 0,2
= 0,2
 , т. к. его значение не указано в условии задачи, т.е. в начальный момент времени этого вещества не было в системе. Следовательно [SO3] = Dc(SO3) = 0,2.
, т. к. его значение не указано в условии задачи, т.е. в начальный момент времени этого вещества не было в системе. Следовательно [SO3] = Dc(SO3) = 0,2.
Находим 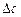 реагентов в соответствии с уравнением (5):
реагентов в соответствии с уравнением (5):
 ,
,
откуда
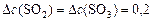 моль/л,
моль/л,
 моль/л.
моль/л.
Рассчитываем равновесные концентрации реагентов:
 моль/л,
моль/л,
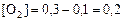 моль/л.
моль/л.
Результат расчетов представим в виде таблицы.
Рассчитываем константу равновесия
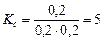 .
.
Таблица 2
   D D 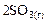
| |||
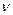
| |||
 , моль/л , моль/л
| 0,4 | 0,3 | |
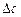 , моль/л , моль/л
| 0,2 | 0,1 | 0,2 |
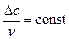
| 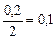
| 
| 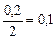
|
| [B], моль/л | 0,2 | 0,2 | 0,2 |
Ответ: 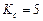 .
.
Пример 2. Рассчитайте  реакции 2С(тв)+О2(г) D 2СО(г), если
реакции 2С(тв)+О2(г) D 2СО(г), если 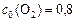 моль/л, а к моменту равновесия прореагировало 27% кислорода.
моль/л, а к моменту равновесия прореагировало 27% кислорода.
Решение.
Реакция гетерогенная, углерод - 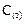 не входит в выражение константы равновесия:
не входит в выражение константы равновесия:

Согласно (4), запишем:
для реагента 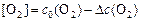 ,
,
для продукта  , т. к.
, т. к. 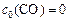 .
.
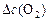 - изменение концентрации
- изменение концентрации  к моменту наступления равновесия рассчитываем из отношения:
к моменту наступления равновесия рассчитываем из отношения:

| – | 100% |
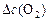
| – | 27% |
 моль/л.
моль/л.
 рассчитываем, воспользовавшись соотношением (5):
рассчитываем, воспользовавшись соотношением (5):
 ;
;
 моль/л.
моль/л.
Определяем равновесные концентрации:
 моль/л,
моль/л,
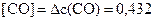 моль/л.
моль/л.
Исходные данные и результат расчетов сводим в таблицу:
Таблица 3
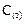   D D 
| |||
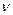
| – | ||
 , моль/л , моль/л
| – | 0,8 | |
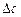 , моль/л , моль/л
| – | 0,216 | 0,432 |
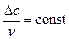
| – | 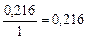
| 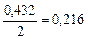
|
| [B], моль/л | – | 0,584 | 0,432 |
Вычисляем  :
:

Ответ:  .
.
Пример 3. В реакторе объемом 5л смешали 8,64 моль азота и 26,13 моль водорода. Рассчитайте константу равновесия реакции:
N2(г) + 3H2(г) D 2NH3(г),
если в момент равновесия в реакторе обнаружено 6,912 моль азота.
Решение.
Реакция гомогенная, выражение константы равновесия:
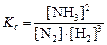
Для определения  необходимо знать равновесные концентрации всех веществ:
необходимо знать равновесные концентрации всех веществ:
для реагентов:  ;
;
 ;
;
для продукта:  .
.
Рассчитаем исходные концентрации веществ-участников реакции. По условию задачи  моль;
моль;  моль,
моль,  , т. к. аммиак не вводили в реактор в начальный момент:
, т. к. аммиак не вводили в реактор в начальный момент:
 моль/л;
моль/л;
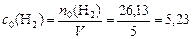 моль/л;
моль/л;
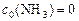
Равновесная концентрация азота вычисляется аналогично:
 .
.
Из уравнения  находим D с (N2):
находим D с (N2):
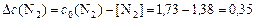 моль/л.
моль/л.
Используя соотношение (5) запишем:
 ,
,
и определяем:
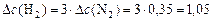 моль/л,
моль/л,
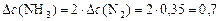 моль/л.
моль/л.
и рассчитываем равновесные концентрации:
 моль/л.
моль/л.
 моль/л.
моль/л.
Рассчитаем значение  :
:
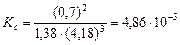 .
.
Ответ: Кс = 4,86×10-3.
1.3. РАСЧЕТ РАВНОВЕСНЫХ КОНЦЕНТРАЦИЙ С ИСПОЛЬЗОВАНИЕМ КОНСТАНТЫ РАВНОВЕСИЯ
Пример 4. Реакция протекает по уравнению 2С(тв)+О2(г) D 2СО(г).
с0(О2)=4 моль/л, Кс =4. Вычислите равновесные концентрации веществ и массовую долю прореагировавшего кислорода.
Решение.
1) Реакция гетерогенная, выражение константы равновесия:
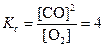
В соответствии с (4) запишем выражения для равновесных концентраций:
[O2] = c0 (O2) - Dc(O2),
[CO] = c0 (CO) + Dc(CO).
Учитывая, что с0(СО)=0моль/л, [CO]=Dc(CO). Для определения изменения концентрации Dc участников реакции запишем в соответствии с (5):
 =const, обозначим эту величину – x.
=const, обозначим эту величину – x.
Отсюда Dc(O2)= x, Dc(CO)=2 x, и тогда [O2]=4 – x и[CO]= 2 x.
Подставляя значения [O2] и [CO] в выражение для константы равновесия, получаем
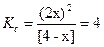 .
.
Решаем уравнение:
4 x 2 = 4(4- x)
4 x 2 + 4 x – 16 = 0, или x 2 + x – 4 = 0
Решаем уравнение относительно x.
D=1-4(-4)=17,
x 1,2=½ (-1±√17),
x 1 = 1,56
x 2 = -2,56. Значение не имеет физического смысла.
Рассчитываем равновесные концентрации:
[O2] = 4 – 1,56 = 2,44 моль/л,
[CO] = 2 · 1,56 = 3,12 моль/л.
2) Рассчитываем массовую долю прореагировавшего кислорода:
c0(O2) – 100%
Dc(O2) – ω %
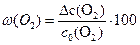 =
= 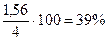 .
.
Ответ: [O2] = 2,44 моль/л, [CO] = 3,12 моль/л,  .
.
Дата публикования: 2015-07-22; Прочитано: 594 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
